
| A. | AlCl3 | B. | KCl | C. | CaCl2 | D. | LiCl |
分析 假设3.8g全部为MgCl2,则生成AgCl为:$\frac{3.8g}{95g/mol}$×2×143.5g/mol=11.48<12.4g,故杂质中氯离子含量应大于MgCl2中氯离子含量,若全部为杂质,生成AgCl的质量应大于12.4g,据此进行解答.
解答 解:若3.8g全部为MgCl2,则生成AgCl为:$\frac{3.8g}{95g/mol}$×2×143.5g/mol=11.48g<12.4g,故杂质中氯离子含量应大于MgCl2中氯离子含量,
MgCl2中Mg、Cl质量之比为24:71,而AlCl3中Al、Cl质量之比为27:35.5×3=18:71,KCl中K、Cl质量之比为78:71,CaCl2中Ca、Cl质量之比为40:71,LiCl中Li、Cl质量之比为14:71,
根据分析可知:氯离子含量大于MgCl2中氯离子含量的为AlCl3、LiCl,
若3.8g全部为AlCl3,生成AgCl沉淀为:$\frac{3.8g}{133.5}$×3×143.5g/mol=12.25g<12.4g,不符合题意;
若杂质3.8g全部为LiCl,生成AgCl为:$\frac{3.8g}{42.5g/mol}$=×2×143.5g/mol=12.8g>12.4g,符合题意,
故选D.
点评 本题考查混合物的计算,题目难度中等,注意用端值法解答,属于易错题目,学生容易考虑氯离子含量大于氯化钙中氯离子含量,忽略若全部为杂质时生成AgCl的质量应大于12.4.


 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 1mol氢气完全燃烧生成液态水放出的热量小于241.8KJ | |
| B. | 1mol水蒸气完全分解成氢气与氧气,需吸收241.8kJ热量 | |
| C. | 2mol氢气与1mol氧气的总能量小于2mol 水蒸气的总能量 | |
| D. | 2mol氢氢键和1mol氧氧键拆开所消耗的能量大于4mol氢氧键成键所放出的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等质量的乙烯和丙烯中含有的共用电子对数 | |
| B. | 等物质的量的水与重水含有的中子数 | |
| C. | 同温、同压、同体积的CO和NO含有的质子数 | |
| D. | 等物质的量的铁和铝分别与足量盐酸完全反应时转移的电子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
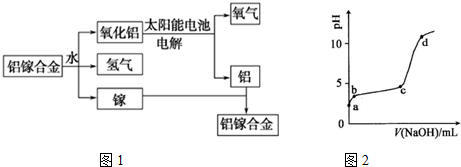
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性:H2SO3>H2CO3 | B. | 熔沸点:HF>HCl | ||
| C. | 碱性:NaOH>Al(OH)3 | D. | 热稳定性:Na2CO3>CaCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入一小块铜片 | B. | 改用等体积 98%的硫酸 | ||
| C. | 用等量铁粉代替铁片 | D. | 改用等体积3mol/L盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
| 离子 | Fe 2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com