
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| c |
| 2 |
| d |
| 2 |
| c |
| 2 |
| d |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |


 С��ſ�ʱ��ҵϵ�д�
С��ſ�ʱ��ҵϵ�д� һ������ϵ�д�
һ������ϵ�д� �Ƹ�С״Ԫ���ֳ������ϵ�д�
�Ƹ�С״Ԫ���ֳ������ϵ�д� �¸��̵�ѧϵ�д�
�¸��̵�ѧϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������ͬ��������֮��н�Ϊ109��28�� |
| B��N-H��Ϊ���Թ��ۼ� |
| C��4��N-H���ļ��ܡ�������ͬ |
| D��N-Hԭ�Ӽ������λ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
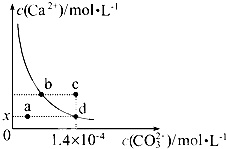 ����ʱ��CaCO3��ˮ�е��ܽ�ƽ��������ͼ��ʾ����֪��25�����ܶȻ�Ϊ2.8��10-9������˵������ȷ���ǣ�������
����ʱ��CaCO3��ˮ�е��ܽ�ƽ��������ͼ��ʾ����֪��25�����ܶȻ�Ϊ2.8��10-9������˵������ȷ���ǣ�������| A����������ˮ��ʹ��Һ��d��䵽a�� |
| B��c��ʱ��̼��Ƴ������� |
| C��x��ֵΪ2��10-5 |
| D��b����d���Ӧ���ܶȻ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���٢ڢۢ� | B���ۢڢ٢� |
| C���ܢۢ٢� | D���ۢڢܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 һ���¶��£�����̼����MCO3��M2+��Mg2+��Ca2+��Mn2+���ij����ܽ�ƽ��������ͼ��ʾ����֪ p��M2+��=-lgc��M2+����p��CO32-��=-lgc��CO32-��������˵����ȷ���ǣ�������
һ���¶��£�����̼����MCO3��M2+��Mg2+��Ca2+��Mn2+���ij����ܽ�ƽ��������ͼ��ʾ����֪ p��M2+��=-lgc��M2+����p��CO32-��=-lgc��CO32-��������˵����ȷ���ǣ�������| A��MgCO3��CaCO3��MnCO3��Ksp�������� |
| B��c������ʾMgCO3��Ϊ��������Һ������ʾCaCO3���г������� |
| C��b��ɱ�ʾCaCO3�ı�����Һ����Ca2+Ũ����CO32-Ũ����� |
| D����100mL MgCO3��CaCO3��MnCO3���͵Ļ����Һ�м�������ŨK2CO3��Һ����������MnCO3������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| Ԫ�� | �����Ϣ |
| X | X�ǵؿ��к�������Ԫ�� |
| Y | YԪ��ԭ�Ӻ���3p�ܼ�����4������ |
| Z | ����Z��������Ϊ14��������Ϊ7 |
| T | T�ĵ�����һ�ֳ����Ľ����������Ƶ�������������Һ�����ڼ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| Mn2+ |
| Mn2+ |
| Mn2+ |
| C2O42- |
| ʵ�� ��� | �ձ��������Լ���������mL�� | �������� | ��Һ�� ɫʱ�� ��s�� | |||
| 0.10mol/L H2C2O4��Һ | ��Ũ�� KMnO4��Һ | H2O | 0.50mol/L ϡ���� | |||
| 1 | 30 | 20 | 30 | 20 | 18 | |
| 2 | 30 | 20 | 30 | 20 | ˮԡ�����¶�65�� | 15 |
| 3 | 30 | 20 | 30 | 20 | ��������MnSO4���� | 3.6 |
| 4 | 30 | 20 | x | 20 | ����5mL 0.10mol/L K2SO4��Һ | 18 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com