
【题目】设NA为阿伏加德罗常数,下列有关说法正确的是
A. 常温常压下,1.8g甲基(—CD3)中含有的中子数为NA
B. 标准状况下,11.2L乙烯和环丙烷(C3H6)的混合气体中,共用电子对的数目为3NA
C. 过量铜与含0.4 mol HNO3的浓硝酸反应,电子转移数大于0.2NA
D. 常温下,1L pH=9的CH3COONa溶液中,发生电离的水分子数为1×10-9 NA
【答案】C
【解析】A,—CD3的摩尔质量为18g/mol,1.8g—CD3物质的量为![]() =0.1mol,1个—CD3中含有9个中子,1.8g—CD3中含有中子物质的量为0.9mol,A项错误;B,n(混合气)=
=0.1mol,1个—CD3中含有9个中子,1.8g—CD3中含有中子物质的量为0.9mol,A项错误;B,n(混合气)=![]() =0.5mol,若11.2L气体全为乙烯,含有的共用电子对物质的量为0.5mol
=0.5mol,若11.2L气体全为乙烯,含有的共用电子对物质的量为0.5mol![]() 6=3mol,若11.2L气体全为环丙烷,含有的共用电子对物质的量为0.5mol
6=3mol,若11.2L气体全为环丙烷,含有的共用电子对物质的量为0.5mol![]() 9=4.5mol,由于乙烯和环丙烷的比例未知,含有的共用电子对物质的量介于3mol和4.5mol之间,B项错误;C,若只发生反应Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,4mol浓HNO3反应转移2mol电子,0.4molHNO3参加反应转移0.2mol电子,若只发生反应3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,8mol稀HNO3反应转移6mol电子,0.4molHNO3参加反应转移0.3mol电子,过量Cu与浓硝酸反应先生成NO2,随着反应的进行HNO3浓度减小,后生成NO,过量Cu与含0.4molHNO3的浓硝酸反应中转移电子物质的量大于0.2mol,C项正确;D,CH3COONa属于强碱弱酸盐,CH3COO-的水解促进水的电离,c(H2O)电离=c(OH-)=1
9=4.5mol,由于乙烯和环丙烷的比例未知,含有的共用电子对物质的量介于3mol和4.5mol之间,B项错误;C,若只发生反应Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,4mol浓HNO3反应转移2mol电子,0.4molHNO3参加反应转移0.2mol电子,若只发生反应3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,8mol稀HNO3反应转移6mol电子,0.4molHNO3参加反应转移0.3mol电子,过量Cu与浓硝酸反应先生成NO2,随着反应的进行HNO3浓度减小,后生成NO,过量Cu与含0.4molHNO3的浓硝酸反应中转移电子物质的量大于0.2mol,C项正确;D,CH3COONa属于强碱弱酸盐,CH3COO-的水解促进水的电离,c(H2O)电离=c(OH-)=1![]() 10-5mol/L,发生电离的水分子物质的量为1
10-5mol/L,发生电离的水分子物质的量为1![]() 10-5mol/L
10-5mol/L![]() 1L=1
1L=1![]() 10-5mol,D项错误;答案选C。
10-5mol,D项错误;答案选C。


科目:高中化学 来源: 题型:
【题目】石英晶体的平面示意图如图所示,它实际上是网状结构,其中硅、氧原子的个数比是m:n,有关叙述正确的是( )(相对原子量Si 28 O 16)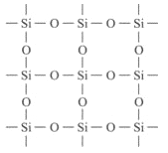
A. 6g该晶体中含有0.1NA个分子
B. m:n=2:1
C. 原硅酸根SiO44—的结构为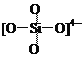 ,则二聚硅酸根离子Si2O7x—中的x=6
,则二聚硅酸根离子Si2O7x—中的x=6
D. 六聚硅酸根[Si6O18]y—中的y=10
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知4NH3 + 5O2 = 4NO + 6H2O,若反应速率分别是ν(NH3)、ν(O2)、ν(NO)、ν(H2O气)(单位:molL-1min-1)。下列关系正确的是 ( )
A. 4/5ν(NH3)=ν(O2) B. 5/6ν(O2)=ν(H2O)
C. 2/3ν(NH3)=ν(H2O) D. 4/5ν(O2)=ν(NO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种离子晶体的晶胞如图,其中阳离子A以![]() 表示,阴离子B以
表示,阴离子B以![]() 表示。
表示。
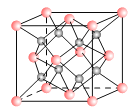
(1)每个晶胞中含A离子的数目为______,含B离子数目为_______。
(2)若A的核外电子排布与Ne相同,B的电子排布与Ar相同,则该离子化合物的化学式是___________;
(3)阳离子周围距离最近的阳离子数为_____,阳离子周围距离最近的阴离子数_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关叙述中正确的是( )
A. 常温下,![]() 的
的![]() 与
与![]() 混合溶液中:
混合溶液中:![]()
B. NaCl溶液和![]() 溶液均显中性,两溶液中水的电离程度相同
溶液均显中性,两溶液中水的电离程度相同
C. 已知![]() 时
时![]() 溶液显碱性,则
溶液显碱性,则![]() 时的电离平衡常数
时的电离平衡常数![]()
D. ![]() 醋酸溶液加少量水稀释
醋酸溶液加少量水稀释![]() 增大
增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学实验在学科中有举足轻重的作用,结合下列实验的图示分析相关的描述正确的是( )
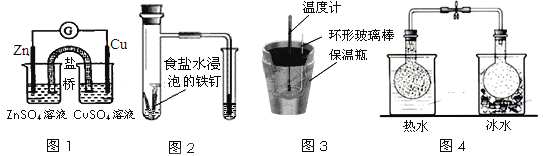
A. 图1:根据用电器(G)中指针的偏转方向可比较Zn、Cu的金属的活泼性
B. 图2:可根据小试管中液面的变化判断铁钉发生了析氢腐蚀
C. 图3:根据温度计读数的变化可测量浓硫酸和NaOH反应的中和热
D. 图4:根据两烧瓶中气体颜色的变化(热水中变深、冰水中变浅)可以判断2NO2(g)![]() N2O4(g)是一个吸热反应
N2O4(g)是一个吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】位于不同主族的四种短周期元素甲、乙、丙、丁,其原子序数依次增大,原子半径r(丁) > r(乙) > r(丙) > r(甲)。四种元素中,只有一种为金属元素,乙和丙原子的最外层电子数之和为丁原子的最外层电子数的3倍。据此推断,下述正确的是
A. 丙的简单氢化物分子内存在氢键
B. 由甲、乙两元素组成的化合物中,只含有极性键
C. 由甲和丙两元素组成的分子不止一种
D. 乙和丁两元素的最高价氧化物的水化物之间能发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用98%、密度为1.84g/cm3的浓硫酸配制0.2mol/L的H2SO4溶液450mL.
(1)需要使用的主要仪器有量筒、烧杯、玻璃棒、___________、__________。
(2)其操作步骤可分解为以下几步:
A.用量筒量取______mL浓硫酸,缓缓注入装有约50mL蒸馏水的烧杯里,并用玻璃棒搅拌。
B.用适量蒸馏水分三次洗涤烧杯和玻璃棒,将每次的洗液都移入容量瓶里。
C.将稀释后的硫酸小心地用玻璃棒引流容量瓶里。
D.检查容量瓶是否漏水。
E.将蒸馏水直接加入容量瓶,至液面接近刻度线1-2cm处。
F.盖紧瓶塞,反复颠倒振荡,摇匀溶液。
G.用胶头滴管向容量瓶里逐滴加入蒸馏水,到液面最低点恰好与刻线相切。
请据此填写:
①完成上述步骤中的空白处。
②补充完成正确的操作顺序(用字母填写):______
( D )→( A )→( )→( )→( )→( )→( F )。
③将浓硫酸在烧杯中稀释后移入容量瓶时,必须_________________方可移液.
(3)试分析下列操作对所配溶液的浓度有何影响:
①量取浓硫酸时眼睛俯视刻度线,会导致所配溶液浓度会________;(填: 偏高、偏低、或无影响,下同)
②定容时,眼睛俯视刻度线,所配溶液浓度会___________;
③定容后,加盖倒转摇匀后,发现溶面低于刻度线,又滴加蒸馏水至刻度。所配溶液浓度会________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对Al2O3、Fe2O3的说法正确的是
A. 都是碱性氧化物 B. 都是白色、难溶于水的固体
C. 都能与NaOH溶液反应 D. 都能与盐酸反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com