
| ���������� | ���� | |
| A | �ⶨͬŨ�ȵ�Na2CO3��Na2SO4��ҺpH��ǰ�ߴ��ں��� | ̼Ԫ�طǽ����������� |
| B | �����ھƾ��ƻ����ϼ����ۻ������� | ���������۵�dz��� |
| C | ȡ����Fe��NO3��2������ˮ�ܽ⣬��ϡ�����ữ���μ�KSCN��Һ����Һ���ɫ | ��Fe��NO3��2�����Ѿ����� |
| D | ������ϡ����ĵ���Һ���Ⱥ�������Ƶ�Cu��OH��2���ȣ�û�к�ɫ���� | �����ڸ������²�ˮ�� |
| A��A | B��B | C��C | D��D |


 ��Ӣ���㿨ϵ�д�
��Ӣ���㿨ϵ�д� Ӧ����㲦ϵ�д�
Ӧ����㲦ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��4KI+O2+2H2O�T4KOH+2I2 | ||||
| B��2CH3COOH+Ca��ClO��2�T2HClO+Ca��CH3COO��2 | ||||
| C��I2+2NaClO3�T2NaIO3+Cl2 | ||||
D��MnO2+4HCl
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��K+��Na+��Cl-��SO42- |
| B��Na+��NH4+��SO42-��HCO3- |
| C��Na+��Ba2+��NO3-��Cl- |
| D��K+��Na+��NO3-��AlO2- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ������㶨���ܱ������У�����2mol CO2��5mol H2��һ�������·�����Ӧ��CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H=-49.0kJ/mol�����CO2��CH3OH��g����Ũ����ʱ��仯��ͼ��ʾ��
������㶨���ܱ������У�����2mol CO2��5mol H2��һ�������·�����Ӧ��CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H=-49.0kJ/mol�����CO2��CH3OH��g����Ũ����ʱ��仯��ͼ��ʾ��| n(CH3OH) |
| n(CO2) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
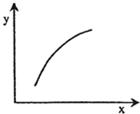 �ڹ̶����������ͨ��2mol A��1mol B���壬һ�������·�����Ӧ��2A��g��+B��g���T3C��g����H��0���ﵽƽ��ı�һ��������x�����������y��һ������ͼ�����ߵ��ǣ�������
�ڹ̶����������ͨ��2mol A��1mol B���壬һ�������·�����Ӧ��2A��g��+B��g���T3C��g����H��0���ﵽƽ��ı�һ��������x�����������y��һ������ͼ�����ߵ��ǣ�������| ѡ�� | x | y |
| A | ���� | A��������� |
| B | �����¶� | ���������ܶ� |
| C | �ټ���A | B��ת���� |
| D | �ټ���C | A��������� |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
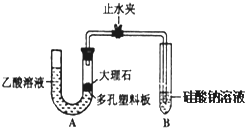 ijУѧϰС���������ʵ�飬̽��CH3COOH��H2CO3��H2SiO3
ijУѧϰС���������ʵ�飬̽��CH3COOH��H2CO3��H2SiO3�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com