
| A���������������ηֱ������������ᷴӦ������ͬ����£�Na2CO3�����Ķ�����̼�� |
| B�������ʵ�����Na2CO3��NaHCO3�ֱ������������ᷴӦ������ͬ����²����Ķ�����̼������ |
| C�������ʵ�����Na2CO3��NaHCO3�ֱ���ͬŨ�ȵ����ᷴӦ��Na2CO3��������������NaHCO3�������������2�� |
| D����ʯ��ˮ����NaHCO3��Һ�л������ɫ������������Na2CO3��Һ��Ҳ�������ɫ���� |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ͭʱ��������Ӧ��Cu2++2e-�TCu | ||
| B������ˮ������ӷ���ʽ��Al3++3H2O?Al��OH��3+3H+ | ||
C����KHSO4��Һ�е���Ba��OH��2��ҺʹpH=7��
| ||
| D��1 L 0.5 mol/Lϡ������1 L 1 mol/L����������Һ��Ӧ�ų�57.3 kJ���ȣ�H2SO4��aq��+2NaOH��aq���TNa2SO4��aq��+2H2O��l����H=-114.6 kJ/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����С�մ�����θ����ࣺHCO3-+H+=CO2��+H2O |
| B�������Ƽӵ���ˮ�У�Na2O+H2O=2Na++2OH-+O2�� |
| C����������������Һ���Ȼ�����Һ��Ӧ��Al3++3OH-=Al��OH��3�� |
| D�����������������OH-+H+=H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��7.1g Cl2������NaOH��Һ��Ӧ��ת�Ƶĵ�����Ϊ0.1NA |
| B���ڳ��³�ѹ�£�5.6L CO�к��е�ԭ����Ϊ0.5NA |
| C��4g NaOH�����к��е���������Ϊ0.3NA |
| D��13.5g Al���������ᷴӦ����H2�ķ�����ΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ | B��ʳ�� |
| C�������� | D���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
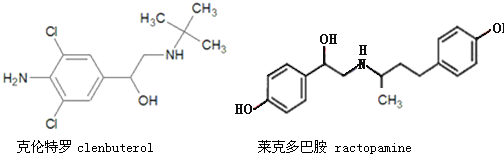
| A�����������ӵķ���ʽΪC12H18ON2Cl2 |
| B�����������ܷ����ӳɡ���������ȥ�ȷ�Ӧ |
| C�������������˶�Ͱ�������FeCl3��Һ���� |
| D�����˶�Ͱ�������NaOH��Ӧ��������Ļ�ѧʽΪC18H20NO3Na3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��5��3 | B��5��4 |
| C��1��1 | D��3��5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ǽ������������������������ |
| B�������Ƿ���ж����ЧӦ������ɢϵ��Ϊ��Һ����Һ�ͽ��� |
| C�����ݵ���ʵ�ˮ��Һ�����Ե�ǿ����������ʷ�Ϊǿ����ʺ�������� |
| D�����ݷ�Ӧ��������������Լ���Ӧǰ����������Ķ��٣��ѻ�ѧ��Ӧ��Ϊ���Ϸ�Ӧ���ֽⷴӦ���û���Ӧ���ֽⷴӦ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com