





 ,该有机物主链为乙苯,在乙基的对位含有1个甲基,该有机物名称为对甲基乙苯,故答案为:对甲基乙苯;
,该有机物主链为乙苯,在乙基的对位含有1个甲基,该有机物名称为对甲基乙苯,故答案为:对甲基乙苯; ,该有机物为3个硝基取代了甲苯苯环上邻位和对位H原子,该有机物为三硝基甲苯,故答案为:三硝基甲苯;
,该有机物为3个硝基取代了甲苯苯环上邻位和对位H原子,该有机物为三硝基甲苯,故答案为:三硝基甲苯; ,该有机物为丙三醇,又名甘油,故答案为:丙三醇;
,该有机物为丙三醇,又名甘油,故答案为:丙三醇; 该有机物为烯烃,含有碳碳双键的最长碳链含有6个C,主链为己烯,碳碳双键在2号C,甲基在4号C,该有机物命名为:4-甲基-2-戊烯,故答案为:4-甲基-2-戊烯;
该有机物为烯烃,含有碳碳双键的最长碳链含有6个C,主链为己烯,碳碳双键在2号C,甲基在4号C,该有机物命名为:4-甲基-2-戊烯,故答案为:4-甲基-2-戊烯; ,该有机物为戊烷,分子中最长碳链含有6个C,主链为己烷,编号称量左端开始,在2、3号C各含有1个甲基,该有机物命名为:2,3-二甲基己烷,故答案为:2,3-二甲基己烷.
,该有机物为戊烷,分子中最长碳链含有6个C,主链为己烷,编号称量左端开始,在2、3号C各含有1个甲基,该有机物命名为:2,3-二甲基己烷,故答案为:2,3-二甲基己烷.


科目:高中化学 来源: 题型:
| A、分子中C、H、O的个数比为1:2:3 |
| B、该有机物的实验式一定为CH2 |
| C、该有机物的相对分子质量为14 |
| D、该分子中可能含有氧元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、黑磷与白磷互为同分异构体 |
| B、黑磷能导电 |
| C、白磷转化为黑磷是物理变化 |
| D、黑磷能在空气中自燃 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 超细氧化镍(NiO)是一种功能材料,已被广泛用于电池电极、催化剂、半导体、玻璃染色剂等方面.工业上常以Ni(NO3)2?6H2O和尿素[CO(NH2)2]为原料制备.
超细氧化镍(NiO)是一种功能材料,已被广泛用于电池电极、催化剂、半导体、玻璃染色剂等方面.工业上常以Ni(NO3)2?6H2O和尿素[CO(NH2)2]为原料制备.查看答案和解析>>
科目:高中化学 来源: 题型:
 计算并填空:
计算并填空:| 1 |
| 2 |
| 化学键 | Si-O | O=O | Si-Si |
| 键能/kJ?mol-1 | X | 498.8 | 176 |
查看答案和解析>>
科目:高中化学 来源: 题型:
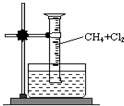 某研究小组为了探究甲烷和氯气反应的情况,设计了几个实验.请填写下列空白:
某研究小组为了探究甲烷和氯气反应的情况,设计了几个实验.请填写下列空白:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com