
【题目】下列反应属于加成反应的是( )
A. 2CH3CH2OH+O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O
B. CH2===CH2+HBr―→CH3CH2Br
C. CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
D. CH4+Cl2![]() CH3Cl+HCl
CH3Cl+HCl
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:
【题目】某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH4为燃料时,该电池工作原理如图,下列说法正确的是
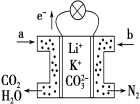
A.a为O2,b为CH4
B.CO 32-向正极移动
C.此电池在常温时也能工作
D.正极电极反应式为2CO2+O2+4e-=2CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.国产大飞机C919用到的氮化硅陶瓷属于新型无机非金属材料
B.用pH试纸测得氯水的pH为2
C.CO、NO、NO2都是大气污染气体,在空气中都能稳定存在
D.铝和重氢氧化钠的![]() 溶液反应的化学方程式:2Al+2NaOD+2
溶液反应的化学方程式:2Al+2NaOD+2![]() 2O=2NaAlO2+D2↑+
2O=2NaAlO2+D2↑+![]() 2↑
2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知短周期元素的离子:aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
A. 原子半径:A>B>D>CB. 原子序数:d>c>b>a
C. 离子半径:C>D>B>AD. 单质的还原性:A>B>D>C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,W、X、Y的最外层电子数之和与Z的最外层电子数相等,W的简单氢化物与Z的单质在集气瓶中混合后,放置在光源下发生反应,气体颜色由黄绿色不断变浅且瓶壁上有油状物生成。下列说法错误的是( )
A.常压下,常见单质的沸点:![]()
B.X离子的电子层结构与Y离子的相同
C.X与Z形成的二元化合物的水溶液呈中性
D.Z分别与W、Y形成的二元化合物所含化学键类型相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】气体A的产量可以衡量一个国家石油化工发展水平。如图是由A为原料生产B的转化关系图,B是一种有香味的液体。
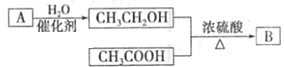
(1)将A通入溴水中,反应方程式__________________________(有机物写结构简式)观察到的实验现象是__________,A分子中官能团是_______。(写名称)
(2)写出CH3CH2OH与CH3COOH反应生成B的化学方程式_________________________,反应类型________
(3)1mol的乙酸与足量的乙醇反应,得到的乙酸乙酯66g,则产率为___________
(4)写出乙醇的一种用途:____________ ;乙烯的一种用途:________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项叙述错误的是
A. 如果硫原子核外电子排布图为![]() ,则违反了泡利原理
,则违反了泡利原理
B. 如果25号Mn元素的基态电子排布式为1s22s22p63s23p63d7,则违反了构造原理
C. 氮原子的核外电子排布图为![]() ,符合洪特规则和泡利原理
,符合洪特规则和泡利原理
D. 泡利原理、洪特规则、构造原理都是对核外电子排布满足能量最低的要求
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下用过量铁片与稀硫酸反应制取氢气,采取下列措施:
①不用铁片,改用铁粉;②加入少量![]() 溶液;③加入少量
溶液;③加入少量![]() 固体;④将稀硫酸换为
固体;④将稀硫酸换为![]() 的硫酸;⑤加入
的硫酸;⑤加入![]() 固体;⑥向
固体;⑥向![]() 中通入HCl气体。 其中可提高
中通入HCl气体。 其中可提高![]() 生成速率的措施有
生成速率的措施有
A.①③④B.①③⑥C.②④⑤D.①④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁铵晶体[(NH4)2SO4·FeSO4·6H2O]又称摩尔盐,难溶于乙醇,常用于定量分析。某实验小组利用工业废铁屑制取摩尔盐,并测定其纯度,工艺流程图如下。
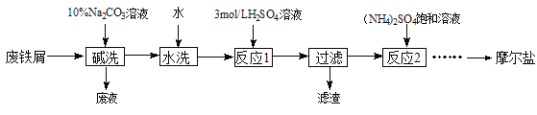
已知:硫酸铵、FeSO4·7H2O、硫酸亚铁铵在水中的溶解度
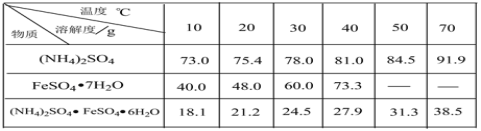
(1)碱洗的目的是_________。
(2)反应1温度需控制在70~75℃,可采取的措施是________。
(3)反应2中常用3 mol·L-1的硫酸调节溶液的pH为1~2,其目的是_______。
(4)请补充完整由反应2所得溶液获得硫酸亚铁铵晶体的实验方案:____、过滤、用乙醇洗涤、低温干燥。
(5)为测定硫酸亚铁铵(NH4)2SO4·FeSO4·6H2O晶体纯度,做了如下实验:
准确称取0.4000g上述硫酸亚铁铵晶体置于锥形瓶中溶解,加适量稀硫酸酸化,用0.0100 mol·L-1 标准KMnO4溶液滴定,当MnO![]() 恰好完全被还原为Mn2+时,消耗KMnO4溶液的体积为20.00 mL。
恰好完全被还原为Mn2+时,消耗KMnO4溶液的体积为20.00 mL。
请回答下列问题:
①滴定终点的现象为____________。
②上述样品中(NH4)2SO4·FeSO4·6H2O晶体(相对分子质量为392)的质量分数为______。
③在上述方案的基础上,下列措施能进一步提高测定准确度的有_____(填字母)。
A.适当增加称量样品的质量 B.用盐酸替代H2SO4溶液
C.用酚酞做指示剂 D.多次实验,取平均值
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com