
| A. | K+、Na+、MnO${\;}_{4}^{-}$、Cl- | B. | K+、Ag+、NO${\;}_{3}^{-}$、Cl- | ||
| C. | Ba2+、Na+、Cl-、SO${\;}_{4}^{2-}$ | D. | Na+、Cu2+、NO${\;}_{3}^{-}$、Cl- |
分析 碱性溶液中存在大量氢氧根离子,
A.四种离子之间不反应,都不与氢氧根离子反应;
B.银离子与硫离子反应生成氯化银沉淀;
C.钡离子与硫酸根离子反应生成硫酸钡沉淀;
D.铜离子与氢氧根离子反应生成氢氧化铜沉淀.
解答 解:碱性溶液中存在大量氢离子,
A.K+、Na+、MnO4-、Cl-之间不反应,都不与氢氧根离子反应,在溶液中能够大量共存,故A正确;
B.Ag+、Cl-之间反应生成AgCl沉淀,在溶液中不能大量共存,故B错误;
C.Ba2+、SO42-之间反应生成硫酸钡沉淀,在溶液中不能大量共存,故C错误;
D.Cu2+与氢氧根离子反应生成氢氧化铜沉淀,在溶液中不能大量共存,故D错误;
故选A.
点评 本题考查离子共存的判断,为高考的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;试题侧重对学生基础知识的训练和检验,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HClO的结构式:H-O-Cl | |
| B. | 质子数为92、中子数为146的U原子:${\;}_{92}^{146}$U | |
| C. | CH2F2的电子式: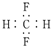 | |
| D. | Cl-的结构示意图: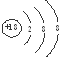 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中最多有4种离子 | B. | 若溶液有颜色,则一定没有OH-、I- | ||
| C. | 若溶液呈碱性,则一定含有Na+ | D. | 该溶液不可能溶解单质铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Cl2是氧化剂,KOH是还原剂 | |
| B. | KClO3是氧化产物,KCl是还原产物 | |
| C. | 该反应中氯气既体现了氧化性又体现了还原性 | |
| D. | 若生成1mol KClO3,则反应中转移10mol e- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 强电解质在溶液中完全电离,其水溶液中不存在分子 | |
| B. | 同一弱电解质溶液,温度不同时,导电能力不同 | |
| C. | 强电解质溶液导电能力不一定比弱电解质溶液的导电能力强 | |
| D. | 强电解质在液态时不一定会导电,但在固态时一定不导电 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有② | B. | ①②③ | C. | ①② | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

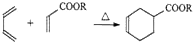

 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$
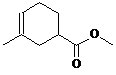 、
、 .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com