
| A、1.2 g镁在足量的氮气中燃烧,镁失去的电子数为0.2NA |
| B、0.1 mol/L氢氧化钠溶液中所含Na+数为0.1NA |
| C、11.2 L二氧化碳中所含有的氧原子数为NA |
| D、46g NO2和N2O4的混合气体中含有的原子个数为3NA |
| m |
| M |
| m |
| M |
| 1.2g |
| 24g/mol |
| 46g |
| 46g/mol |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硝酸不稳定,见光或受热就会分解 |
| B、稀硝酸是弱酸,浓硝酸是强酸 |
| C、铜与稀硝酸反应生成二氧化氮 |
| D、稀硝酸是弱氧化剂,浓硝酸是强氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、快 | B、慢 | C、相等 | D、无法比较 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、苯与溴水混合振荡,水层颜色变浅,是由于苯与溴发生取代反应 |
| B、煤中含有苯和甲苯,可用先干馏后分馏的方法将它们分离出来 |
| C、蛋白质溶液中加入饱和(NH4)2SO4溶液后蛋白质会析出,再加水不溶解 |
| D、CH3COOH 和HCOOCH3是同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=3的二元酸H2R溶液与pH=11的NaOH溶液混合后,混合溶液的pH=7则溶液中c(R2-)>c(Na+)>c(H+)=c(OH-) |
| B、同浓度的下列溶液:①NH4A1(SO4)2;②NH4Cl;③NH3?H2O其中c(NH4+) 由大到小的顺序是:①>②>③ |
| C、物质的量浓度相同的弱酸HX与NaX等体积混合后,溶液中有下列粒子浓度关系:则c(Na+)>c(X-)>c(H+)>c(OH-) |
| D、25℃时0.1mol?L-1NaHCO3溶液中:2(H2CO3)+c(H+)=c(CO32-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、阿伏加德罗常数的符号为NA,其近似值为6.02×1023 mol-1 |
| B、等物质的量的O2与O3,所含氧原子数相同 |
| C、在0.5 mol Na2SO4中,含有的Na+数约是6.02×1023 |
| D、摩尔是物质的量的单位 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 俗称 | 醋酸 | 石炭酸 | 福尔马林 | 四氯化碳 |
| 成分 | CH3COOH | 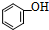 | HCHO | CCl4 |
| 用途 | 调味剂 | 环境消毒 | 防腐剂 | 灭火 |
| 选项 | A | B | C | D |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com