
在复杂的体系中,确认化学反应先后顺序有利于解决问题,下列化学反应先后顺序判断
正确的是
A.含等物质的量的AlO2-、OH-、CO32-的溶液中,逐滴加入盐酸:AlO2-、OH-、CO32-
B.含等物质的量的FeBr2、Fel2的溶液中,缓慢通入氯气:I-、Br-、Fe2+
C.含等物质的量的Ba(OH)2、KOH的溶液中,缓慢通入CO2:KOH、Ba(OH)2、K2CO3、BaCO3
D.含等物质的量的Fe3+、Cu2+、H+的溶液中加入锌粉:Fe3+、Cu2+、H+、Fe2+
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:
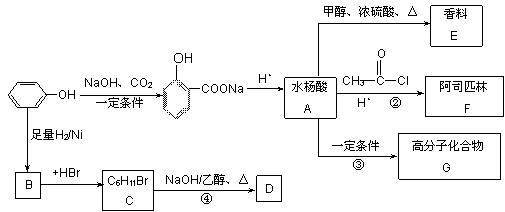
 苯酚是一种重要的化工原料,以下是以苯酚为原料,生产阿司匹林、香料和高分子化合物的合成线路图。
苯酚是一种重要的化工原料,以下是以苯酚为原料,生产阿司匹林、香料和高分子化合物的合成线路图。
 (3)R—OH+HBr
(3)R—OH+HBr R—Br+H2O
R—Br+H2O
(1)写出反应类型:反应④属于_____________反应,反应③属于________________反应。
(2)写出下列有机物的结构简式:E___________、G_____________、F____________。
(3)可以检验阿司匹林样品中含有水杨酸的试剂是__________(填写字母)。
A.碳酸氢钠溶液 B.氯化铁溶液 C.红色石蕊试液 D.新制氢氧化铜悬浊液
(4)与阿司匹林互为同分异构体的物质有多种,请按以下要求写出阿司匹林的一种同分异构体:①苯环上有两个对位的取代基;②能发生银镜反应;③含有酯基和羧基的有机物________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
自然界地表层原生铜的硫化物经氧化、淋滤作用后变成CuSO4溶液,向地下层渗透,遇到难溶的ZnS或PbS,慢慢转化为铜蓝(CuS)。下列分析正确的是
A.CuS的溶解度大于PbS的溶解度,Ksp(ZnS)<Ksp(CuS)
B.原生铜的硫化物具有还原性,而铜蓝没有还原性
C.CuSO4与ZnS反应的离子方程式是Cu2++S2-=CuS↓
D.整个过程涉及的反应类型有氧化还原反应和复分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
设阿伏加德罗常数的值为NA,下列说法中正确的是
A.1 mol 苯乙烯中含有的C=C数为4 NA
B.2.8 g 乙烯和丙烯的混合气体中所含碳原子数为0.2 NA
C.0.1 mol CnH2n+2中含有的C—C键数为0.1n NA
D.标准状况下,2.24 L CCl4含有的分子数为0.1 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
取8 g某有机物A(相对分子质量为32)在氧气中完全燃烧,生成物中只有11 g CO2和9 g H2O。通过计算推断:
(1)该有机物A中含有的元素。
(2)该有机物的分子式及可能的结构简式
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇是重要的化学工业基础原料和清洁液体燃料。工业上可利用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:


⑴反应②是 (填“吸热”或“放热”)反应。
 ⑵某温度下反应①中H2的平衡转化率(a)与体系总压强(P)的关系,如图所示。则平衡状态由A变到B时,平衡常数K(A) K(B)(填“>”、“<”或“=”)。据反应①与②可推导出K1、K2与K3之间的关系,则K3= (用K1、K2表示)。
⑵某温度下反应①中H2的平衡转化率(a)与体系总压强(P)的关系,如图所示。则平衡状态由A变到B时,平衡常数K(A) K(B)(填“>”、“<”或“=”)。据反应①与②可推导出K1、K2与K3之间的关系,则K3= (用K1、K2表示)。
⑶在3 L容积可变的密闭容器中发生反应②,已知c(CO)与反应时间t变化曲线Ⅰ如图所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ。
当曲线Ⅰ变为曲线Ⅱ时,改变的条件是 。
当曲线Ⅰ变为曲线Ⅲ时,改变的条件是 。
⑷甲醇燃料电池有着广泛的用途,同时Al-AgO电池是应用广泛的鱼雷电池,其原理如图所示。该电池的负极反应式是 。
⑸一定条件下甲醇与一氧化碳反应可以合成乙酸。通常状况下,将a mol/L的醋酸与b mol/LBa(OH)2溶液等体积混合,反应平衡时,2c(Ba2+)= c(CH3COO-),用含a和b的代数式表示该混合溶液中醋酸的电离常数为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于有机化合物的说法正确的是( )
A.乙酸和乙酸乙酯可用Na2CO3溶液加以区别 B.汽油、乙烯均为石油分馏产品
C.可以用分液的方法分离硝基苯和苯 D.有机化合物都能燃烧
查看答案和解析>>
科目:高中化学 来源: 题型:
 实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏(如下图所示),得到含有乙醇、乙酸和水的乙酸乙酯粗产品。请回答下列问题:
实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏(如下图所示),得到含有乙醇、乙酸和水的乙酸乙酯粗产品。请回答下列问题:
(已知:乙醇、乙酸、乙酸乙酯的沸点依次是78.4℃、118℃、77.1℃)
(1)在烧瓶中除了加入乙醇、浓硫酸和乙酸外,还应放入几块碎瓷片,其目的是_________________________________。
(2)在烧瓶中加入一定比例的乙醇和浓硫酸的混合液的方法是:_____________________________________________。
(3)在该实验中,若用1 mol乙醇和1 mol乙酸在浓硫酸作用下加热,充分反应,能否生成1mol乙酸乙酯?________,原因是__________________________________。
(4)现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,下图是分离操作步骤流程图。请在图中圆括号内填入适当的试剂,在方括号内填入适当的分离方法。

试剂a是__________,试剂b是__________;分离方法①是________,分离方法②是________,分离方法③是______。
(5)在得到的A中加入无水碳酸钠粉末,振荡,目的是________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com