
| A. | 碳酸钠固体 | B. | 水 | C. | 硫酸钾溶液 | D. | 硫酸铜固体 |
分析 为了减缓反应进行的速度,但又不影响生成氢气的总量,可降低氢离子浓度,但氢离子的总物质的量不变,以此解答该题.
解答 解:A.加入碳酸钠,消耗氢离子,反应速率降低,生成氢气总量减小,故A错误;
B.加入水,氢离子浓度减小,反应速率减小,但生成氢气的总量不变,故B正确;
C.硫酸钾溶液,硫酸钾不参与反应,但加入的水可使氢离子浓度减小,反应速率减小,但生成氢气的总量不变,故C正确;
D.加入硫酸铜,锌置换出铜,形成原电池反应,加快反应速率,故D错误.
故选BC.
点评 本题考查化学反应速率的影响,侧重于基础知识的考查,为高考高频考点,难度不大,注意把握题目要求,易错点为D,注意原电池反应.


科目:高中化学 来源: 题型:选择题
 某有机物的结构简式图,取Na、NaOH、H2分别与等物质的量的该物质恰好反应(反应时可加热煮沸),则Na、NaOH、H2三种物质的物质的量之比为( )
某有机物的结构简式图,取Na、NaOH、H2分别与等物质的量的该物质恰好反应(反应时可加热煮沸),则Na、NaOH、H2三种物质的物质的量之比为( )| A. | 3:2:5 | B. | 3:3:4 | C. | 3:2:4 | D. | 1:1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,14g氮气含有的核外电子数为5NA | |
| B. | 32 g S8单质(S8分子结构如图)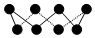 中含有的S-S键个数为8NA 中含有的S-S键个数为8NA | |
| C. | 17g的氢氧根离子中含有的电子数为9NA | |
| D. | 常温下,4.6gNa和足量的O2完全反应失去电子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大于9a×10-3mol,小于18a×10-3mol | B. | 都等于9a×10-3mol | ||
| C. | 都等于18a×10-3mol | D. | 都小于9a×10-3mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S(s)在O2(g)中燃烧的反应是放热反应 | |
| B. | S(g)+O2(g)═SO2(g)△H=b kJ•mol-1,则a<b | |
| C. | 1 mol SO2(g)所具有的能量低于1 mol S(s)与1 mol O2(g)所具有的能量之和 | |
| D. | 16 g固体硫在氧气中充分燃烧,可放出148.6 kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Al→Al2O3→A1(OH)3→NaAlO2 | B. | Fe→FeCl2→Fe(OH)2→Fe(OH)3 | ||
| C. | Si→SiO2→Na2SiO3→H2SiO3 | D. | Na→Na2O2→Na2CO3→NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加适量的KI溶液 | B. | 通入溴蒸气 | ||
| C. | 加入适量的NaBr溶液 | D. | 加入适量的NaOH溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com