
| 1 |
| 2 |
| cmol/L |
| 2min |
| c |
| 2 |
| c |
| 2 |
| 1 |
| 2 |
| 0.04 | ||
0.01��
|



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
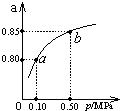
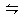 N2O4������˵����֤����Ӧ�Ѵ�ƽ��״̬����
N2O4������˵����֤����Ӧ�Ѵ�ƽ��״̬���� �鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���٢� | B���٢�? | C���ڢ� | D���ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��v��C��=v��D��=0.25mol?L-1?s-1 |
| B��z=2 |
| C��B��ת����Ϊ25% |
| D��C���������Ϊ28.6% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���Ҵ�����֬ | B���ƾ���ˮ | C������ˮ | D�����ͺ�ú�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
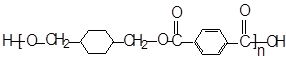
 ��CH3+Cl2��
��CH3+Cl2�� ��CH2Cl+HCl
��CH2Cl+HCl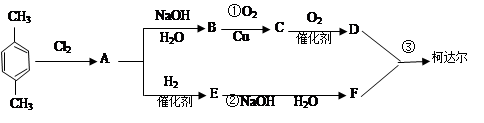
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����ͷ�����ڿ�ǻ��Խ��Խ������Ϊ���Ǻ��еĵ��۷�����������Ӧ |
| B�����ࡢ��֬�������ʶ��ܷ���ˮ�ⷴӦ |
| C�������͡�ţ�͡������Ͷ��������� |
| D�������Ƿ��ӽṹ��ֻ��һ��ȩ���������ǵ��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com