
【题目】I .甲、乙、丙3位同学,在已知盐酸是强酸的基础上,通过实验验证醋酸是弱酸,分别设计了如下实验方案:
甲:分别准确配制0.1 mol/L的盐酸和醋酸各250 mL,再用pH试纸分别测定两溶液的pH。
乙:分别准确配制0.1 mol/L的盐酸和醋酸各250 mL。各取出20 mL于锥形瓶中,逐滴加入0.1 mol/L标准NaOH溶液(不需配制),分别记录恰好中和时用去NaOH溶液的体积。
丙:分别准确配制pH=1的盐酸和醋酸各250 mL。各取出10 mL加水稀释到100 mL后比较稀释后溶液的pH。回答下列问题:
(1)甲同学的实验结果为盐酸和醋酸的pH分别为pH1和pH2,则pH1_____pH2(填“>”“<”或“=”),所以此实验方案________(填“可行”或“不可行”)。
(2)乙同学的实验结果为盐酸和醋酸分别用去NaOH溶液V1 mL和V2 mL,则V1____V2(填“>”“<”或“=”),所以此实验方案______(填“可行”或“不可行”)。
(3)丙同学的实验方案不可行的原因是____________________________________。
II. 测定Na2S2O3样品纯度。
取10.0 g Na2S2O3·5H2O样品,配成 250mL溶液,准确量取25.00 mL溶液,以淀粉作指示剂,用0.1000 mol·L-1碘的标准溶液滴定。三次平行实验测得的数据如下:
实验序号 | 消耗标准溶液体积/mL |
1 | 19.98 |
2 | 17.90 |
3 | 18.10 |
已知:2Na2S2O3+I2=Na2S4O6+2NaI
①滴定终点的颜色为__________________。
②该Na2S2O3·5H2O样品的纯度为___%(保留2位小数)(已知Na2S2O3·5H2O的M=248g mol·-1)。
③若样品中含Na2SO3(还原性:SO32->I-),则测得的结果_______(填“偏高”“偏低”或“无影响”)
【答案】< 可行 = 不可行 无法准确配制pH=1的醋酸 蓝色 89.28 偏高
【解析】
I .(1)醋酸是弱电解质,部分电离;
(2)同体积、同浓度的盐酸和醋酸,盐酸和醋酸物质的量相等。
(3)醋酸是弱电解质,无法准确配制250 mL pH=1的醋酸;
II. ①碘单质能使淀粉变蓝;
②第一次实验超出正常的误差范围,根据用第二次、第三次实验数据,平均消耗碘的标准溶液18.00mL,根据反应方程式2Na2S2O3+I2=Na2S4O6+2NaI计算样品的纯度;
③Na2SO3,Na2SO3能被碘单质氧化;
I .(1)醋酸是弱电解质,部分电离,同浓度的盐酸和醋酸,氢离子浓度盐酸大于醋酸,所以pH1<pH2;所以此实验方案可行;
(2)同体积、同浓度的盐酸和醋酸,盐酸和醋酸物质的量相等,所以恰好中和时用去NaOH溶液的体积相同,所以此实验方案不可行。
(3)醋酸是弱电解质,无法准确配制250 mL pH=1的醋酸,所以丙同学的实验方案不可行;
II.①用0.1000 mol·L-1碘的标准溶液,滴定Na2S2O3溶液,滴定终点时,有碘单质剩余,溶液颜色为蓝色;
②设样品中Na2S2O3的物质的量为xmol;
2Na2S2O3+I2=Na2S4O6+2NaI
2 1
x 0.018L×0.1 mol·L-1×![]()
x=0.036mol;
样品中Na2S2O3·5H2O的质量为0.036mol×248g mol·-1=8.928g,该Na2S2O3·5H2O样品的纯度为8.928g ÷10.0 g×100%=89.28%;
③Na2SO3,Na2SO3能被碘单质氧化,若样品中含Na2SO3,消耗标准碘液的体积偏大,则测得的结果偏高。


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案科目:高中化学 来源: 题型:
【题目】某实验小组欲制取氧化铜并证明氧化铜能加快氯酸钾的分解,进行了如下实验:
(一)制取氧化铜
①往盛有一定量CuCl2溶液的烧杯中逐滴加入NaOH溶液,直至不再产生沉淀,然后将烧杯中的物质转移到蒸发皿中,加热至沉淀全部变为黑色。
②将步骤①所得的黑色沉淀过滤、洗涤,晾干后研细备用。
(1)在实验过程中,若未加入NaOH溶液,直接将CuCl2溶液转移到蒸发皿中加热,最后也能得到黑色沉淀,试分析其原因__________。
(2)写出检验步骤②中沉淀是否洗涤干净的操作__________________。
(二)为证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较,用下图装置进行实验,每次实验时均收集25ml气体,其他可能影响实验的因素均已忽略,实验数据见下表:

实验序号 | KClO3质量 | 其他物质质量 | 待测数据 |
③ | 1.2g | 无其他物质 | a |
④ | 1.2g | CuO 0.5g | b |
⑤ | 1.2g | MnO20.5g | c |
(3)写出氯酸钾分解反应的化学方程式,并用双线桥表示电子转移的方向和数目________。
(4)上述实验中的“待测数据”是指___________________。
(5)图中量气装置B由干燥管、乳胶管和50mL滴定管改造后组装面成,此处用滴定管是________(填“酸式”或“碱式”)滴定管。
(6)若实验证明氧化铜加快氯酸钾的分解效果比用二氧化锰差,请结合上表的实验效果数据,在坐标图中分别画出使用CuO、MnO2作催化剂时产生氧气的体积[V(O2)]随时间(t)变化的曲线(注明必要的标识)________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验。
Ⅰ.(1)将钠、钾、镁、铝各1 mol分别投入到足量的0.1 mol·L-1的盐酸中,试预测实验结果:__________与盐酸反应最剧烈,__________与盐酸反应最慢。
(2)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理?并说明理由:_______,________________。
Ⅱ.利用下图装置可以验证非金属性的变化规律。
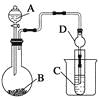
(3)仪器A的名称为________,干燥管D的作用是_____________________________。
(4)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫:装置A、B、C中所装药品分别为________、________、________,装置C中的实验现象为有淡黄色沉淀生成,离子方程式为_________________________。
(5)若要证明非金属性:C>Si,则A中加________、B中加Na2CO3、C中加________,观察到C中溶液的现象为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】保持恒温、恒容,在某密闭容器中发生反应:2A(g)+2B(g)![]() C(g)+3D(g)。现分别从两条途径建立平衡:Ⅰ——从正反应开始,A、B的起始物质的量均为2mol ;Ⅱ——从逆反应开始,C、D的起始物质的量分别为2mol和6mol。以下叙述中正确的是
C(g)+3D(g)。现分别从两条途径建立平衡:Ⅰ——从正反应开始,A、B的起始物质的量均为2mol ;Ⅱ——从逆反应开始,C、D的起始物质的量分别为2mol和6mol。以下叙述中正确的是
A.Ⅰ、Ⅱ两种途径从反应开始到平衡状态所消耗的时间相同
B.Ⅰ、Ⅱ两种途径最终达到平衡时,体系的总压强相等
C.Ⅰ、Ⅱ两途径最终达到平衡时,体系内A的物质的量分数相同
D.Ⅰ、Ⅱ两途径最终达到平衡时,体系内A的浓度相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】稀氨水中存在着下列平衡:NH3·H2O![]() NH4++OH-,若要使平衡向逆反应方向移动,同时使c(OH-)增大,应加入的物质或采取的措施是( )
NH4++OH-,若要使平衡向逆反应方向移动,同时使c(OH-)增大,应加入的物质或采取的措施是( )
①NH4Cl固体 ②硫酸 ③NaOH固体 ④水 ⑤加热 ⑥少量MgSO4固体
A. ①②③⑤B. ③C. ③④⑥D. ③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.pH相等的四种溶液:![]()
![]()
![]()
![]() ,则四种溶液的溶质的物质的量浓度由小到大顺序为:
,则四种溶液的溶质的物质的量浓度由小到大顺序为:![]()
B.除去氯化铜溶液中的氯化铁杂质,可在溶液中加入过量的氧化铜,过滤达到除杂的目的
C.改变温度一定会导致已达化学平衡的反应发生移动
D.在一个固定容积的密闭容器中存在可逆反应![]() ,当混合气体的平均摩尔质量不再改变时,可逆反应一定达到平衡
,当混合气体的平均摩尔质量不再改变时,可逆反应一定达到平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知元素X的原子核外次外层电子数为2、价电子数4,其气态氢化合物的密度为![]() 标准状况
标准状况![]() 。下列说法不正确的是
。下列说法不正确的是
A.基态X原子的价电子排布图为![]()
B.该化合物分子中含有2个![]() 键,3个
键,3个![]() 键
键
C.该化合物分子中X原子的杂化方式为![]() 杂化
杂化
D.该元素的最高价氧化物的空间构型为直线形
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列5种元素的电离能数据![]() 单位:
单位:![]()
元素符号 |
|
|
|
|
Q | 2080 | 4000 | 6100 | 9400 |
R | 500 | 4600 | 6900 | 9500 |
S | 740 | 1500 | 7700 | 10500 |
T | 580 | 1800 | 2700 | 11600 |
V | 420 | 3100 | 4400 | 5900 |
它们的氯化物的化学式,最可能正确的是
A.![]() B.RClC.
B.RClC.![]() D.TCl
D.TCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂。其中没食子儿茶素(EGC)的结构如下图所示。关于EGC的下列叙述中正确的是
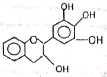
A.分子中所有的原子共面
B.1mol EGC与5mol NaOH恰好完全反应
C.易发生氧化反应和取代反应,可发生加成反应
D.遇FeCl3浴液不发生显色反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com