
| A、c(H+)=1×10-2mol?L-1的溶液:Na+、NH4+、CO32-、SO42- |
| B、水电离产生的c(H+)=1×10-12mol/L溶液:Fe2+、Ca2+、I-、NO3- |
| C、含有大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- |
| D、能使pH试纸变深蓝色的溶液中:Na+、AlO2-、S2-、CO32- |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32- |
| B、加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- |
| C、先加入KSCN溶液无明显现象,再加入氯水,溶液变血红色,一定有Fe2+ |
| D、加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,稀释0.1 mol/L的氨水,溶液中c(OH-)、c(NH4+)、c(H+)均下降 |
| B、常温下,c(NH4+)相等的①(NH4)2SO4 ②(NH4)2Fe(SO4)2 ③NH4Cl ④(NH4)2CO3溶液中,溶质物质的量浓度大小关系是:②<①<④<③ |
| C、pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
| D、当溶液中存在的离子只有Cl-、OH-、NH4+、H+时,该溶液中离子浓度大小关系可能为c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
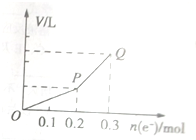 用惰性电极电解硫酸铜溶液,整个过程转移电子的物质的量与产生气体总体积的关系如图所示(气体体积均在相同状况下测定).欲使溶液恢复到起始状态,可向溶液中加入( )
用惰性电极电解硫酸铜溶液,整个过程转移电子的物质的量与产生气体总体积的关系如图所示(气体体积均在相同状况下测定).欲使溶液恢复到起始状态,可向溶液中加入( )| A、0.1molCuO |
| B、0.1molCuCO3 |
| C、0.1molCu(OH)2 |
| D、0.05molCu2(OH)2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 将1molCO和2molH2充入一容积为1L的密闭容器中,分别在250℃、T℃下发生反应:CO(g)+2H2(g)?CH3OH(g)△H=a KJ?mol-1,如图所示,下列分析中正确的是( )
将1molCO和2molH2充入一容积为1L的密闭容器中,分别在250℃、T℃下发生反应:CO(g)+2H2(g)?CH3OH(g)△H=a KJ?mol-1,如图所示,下列分析中正确的是( )| A、250℃时,0~10minH2反应速率为0.015mol?(L?Min)-1 |
| B、平衡时CO的转化率:T℃时小于250℃时 |
| C、a>0 |
| D、平衡常数K:T℃时大于250℃ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com