
| 混合物 | 试剂 | 分离方法 | |
| A | 苯(苯酚) | 溴水 | 过滤 |
| B | 乙烷(乙烯) | 酸性高锰酸钾 | 洗气 |
| C | 乙酸乙酯(乙酸) | NaOH溶液 | 蒸馏 |
| D | 溴苯(液溴) | NaOH溶液 | 渗析 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.溴、三溴苯酚易溶于苯;
B.乙烯被酸性高锰酸钾氧化生成二氧化碳气体;
C.二者都与氢氧化钠溶液反应;
D.溴与氢氧化钠反应,液溴不溶于水.
解答 解:A.溴与苯酚反应生成三溴苯酚,溴、三溴苯酚都易溶于苯,不能分离,应用氢氧化钠溶液除杂,故A错误;
B.乙烯被酸性高锰酸钾氧化生成二氧化碳气体,引入新杂质,应用溴水除杂,故B错误;
C.二者都与氢氧化钠溶液反应,应用饱和碳酸钠溶液除杂,故C错误;
D.溴与氢氧化钠反应,液溴不溶于水,可用于除杂,故D正确.
故选D.
点评 本题考查混合物分离提纯方法的选择和应用,为高频考点,把握物质的性质及性质差异选择分离试剂及方法为解答的关键,注意物质的性质及发生的化学反应,题目难度不大.


科目:高中化学 来源: 题型:填空题
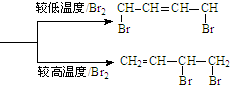
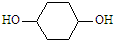 ,写出正确的合成路线:
,写出正确的合成路线: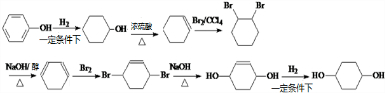 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1 (NH4)2Fe(SO4)2溶液中:K+、Cu2+、Cl-、MnO4- | |
| B. | 0.1 mol•L-1 FeCl2溶液:K+、Na+、SO42-、NO3- | |
| C. | 使甲基橙变红色的溶液:NH4+、Cu2+、ClO-、Cl- | |
| D. | 0.1mol•L-1NaHCO3溶液:K+、AlO2-、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ⅦA族元素是同周期中原子半径最大的元素 | |
| B. | ⅦA族元素其简单阴离子的核外电子层数等于该元素所在的周期数 | |
| C. | ⅦA族元素的最高正价都是+7价 | |
| D. | ⅦA族元素是同周期中非金属性最弱的元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
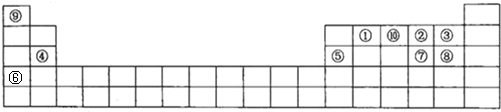
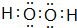 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:多选题
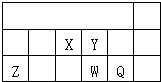 短周期元素X、Y、Z、W、Q在元素周期表中的相对位置R如上表所示;下列说法
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置R如上表所示;下列说法| A. | X的最高价氧化物的水化物不能与它的氢化物反应 | |
| B. | Y原子的电子总数是其K层电子数的3倍 | |
| C. | Z在高温下可与铁的氧化物发生铝热反应 | |
| D. | Q的单质能与W的氢化物发生置换反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com