
| 催化剂 |
| △ |

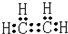 ,故答案为:
,故答案为: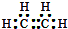 ;
;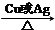 CH3CH2OH,
CH3CH2OH, ,
,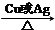 2CH3CHO+2H2O;
2CH3CHO+2H2O;


科目:高中化学 来源: 题型:
| A、NH4+、Al3+、SO42-、NO3- |
| B、Ba2+、K+、Cl-、SO42- |
| C、K+、MnO4-、NH4+、NO3- |
| D、Mg2+、K+、CO32-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在理解概念的基础上,理清概念之间的相互关系,构建完整的知识体系是学习化学的重间的相互关系.中学化学常见晶体类型有:离子晶体如NaOH、KNO3等;
在理解概念的基础上,理清概念之间的相互关系,构建完整的知识体系是学习化学的重间的相互关系.中学化学常见晶体类型有:离子晶体如NaOH、KNO3等;| A | B | C | ||
| 晶体类别 | 分子晶体 | 原子晶体 | 金属晶体 | |
| 实例的化学式 | Na |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 向2L密闭容器中加入一定量的A、B、C三种气体,一定条件下发生反应,各物质的物质的量随时间变化如图甲所示[t0~15s阶段n(B)未画出].图乙为t2时刻后改变条件平衡体系中反应速率随时间变化的情况,且四个阶段所改变的外界条件均不同.已知t3~t4阶段为使用催化剂.观察如图,回答以下问题:
向2L密闭容器中加入一定量的A、B、C三种气体,一定条件下发生反应,各物质的物质的量随时间变化如图甲所示[t0~15s阶段n(B)未画出].图乙为t2时刻后改变条件平衡体系中反应速率随时间变化的情况,且四个阶段所改变的外界条件均不同.已知t3~t4阶段为使用催化剂.观察如图,回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 混合液为酸性 | |
| 混合液为中性 | |
| 混合液为碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2O、Na2O2组成元素相同,推出与水反应产物也完全相同 |
| B、SO2和湿润的Cl2都有漂白性,推出二者混合后漂白性更强 |
| C、H2CO3的酸性比HClO强,推出CO2通入NaClO溶液中能生成HClO |
| D、根据铜与浓硫酸可以制取SO2,推出常温下铁与浓硫酸也可以制取SO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com