
C��N��S����Ҫ�ķǽ���Ԫ�أ���Ҫ��ش��������⣺
��1���̵����к��е�CO��SO2����Ҫ����Ⱦ����ڴ��������½�����ת��ΪS��s����CO2���˷�Ӧ���Ȼ�ѧ����ʽΪ______________________________________��
��֪��CO��g��+1/2O2��g��=CO2��g�� ��H=��283��0kJ��mol��1��
S��s��+O2=SO2��g�� ��H=��296��0 kJ��mol��1
��2����ס���������Ϊ1L���ܱ������У��ֱ����5mol SO2��3mol O2��������Ӧ��
2 SO2 ��g����O2 ��g�� 2SO3��g�� ��H��0�����������¶�ΪT1�������·�Ӧ���ﵽƽ��ʱSO3�����ʵ���Ϊ4��5mol�����������¶�ΪT2�������·�Ӧ���ﵽƽ��ʱSO3�����ʵ���Ϊ4��6mol��
2SO3��g�� ��H��0�����������¶�ΪT1�������·�Ӧ���ﵽƽ��ʱSO3�����ʵ���Ϊ4��5mol�����������¶�ΪT2�������·�Ӧ���ﵽƽ��ʱSO3�����ʵ���Ϊ4��6mol��
��T1________T2������������������������з�Ӧ��ƽ�ⳣ��K=___________��
��3����ͼ��ʾ��A�Ǻ��ݵ��ܱ�������B��һ������ɱ�ij������ҡ����ֺ��£��ر�K2���ֱ�1 mol N2��3mol H2ͨ��K1��K3����A��B�У������ķ�ӦΪ��
N2��g��+3H2��g��  2NH3��g������ʼʱA��B�������ͬ��Ϊa L��
2NH3��g������ʼʱA��B�������ͬ��Ϊa L��

������ʾ��ͼ��ȷ���Ҽ���˵��A�����з�Ӧ�ﵽƽ��״̬������˵��B�����з�Ӧ�ﵽƽ��״̬����_ __��
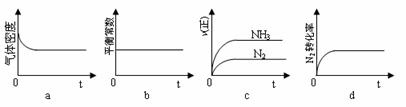
������A�з�Ӧ����ƽ��ʱ����ʱ��t s���ﵽƽ���������ѹǿ��Ϊԭ����5/6����ƽ����Ӧ����v��H2��=____��
��4����0��1mol�����ֱ�ͨ��1L pH=1�����ᡢ����ʹ�����Һ�У���ȫ��Ӧ������Һ��NH4+����Ũ�ȷֱ�Ϊc1��c2��c3��������Ũ�ȴ�С�Ĺ�ϵΪ_______ ����c1��c2��c3�ͣ�����������ʾ������֪�������Һ�����ԣ�������CH3COOH��Ka��1��10��5 mol��L��1������¶���0��1 mol��L��1��NH4Cl��Һ��pHΪ_________��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������ȷ����
A���������п���������� B���ֹ����Դ�������ӣ��ֹܿɱ�����
C�����뺣�ڵĸ���բ����װͭ��ɷ�ֹբ�ű���ʴ
D�������������ⸯʴʱ��������Ӧ��Fe��3e��=Fe3+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ʾ���ڴ�����ȼ��ʵ��ʱ������˿�Ƴ�����״������ҪĿ����(����)
A�������˿������
B����߷�Ӧ�¶�
C������Ӧ�ĽӴ���
D��ʹƿ�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���д�ʩ����ʵ��������������ԭ�����͵��� ( )
A�����Ƶ���ˮ�ڹ�������ɫ��dz
B��Fe(SCN)3��Һ�м���6mol/L NaOH��Һ����ɫ��dz
C���ںϳɰ��ķ�Ӧ�У����»��ѹ�����ڰ��ĺϳ�
D��H2��I2��HIƽ��������ѹ����ɫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����й�ʵ���˵������ȷ���� ( )
A���ڲⶨ�кͷ�Ӧ�ķ�Ӧ��ʵ���У�Ҫ��ȡ����¶�
B���к͵ζ�ʵ���У�ϴ�������ƿ����Ҫ����
C����CH3COONa��Һ�е���ʯ����Һ����Һ����
D�����ɫZnS�����ϵμ�CuSO4��Һ��������Ϊ��ɫ��˵��Ksp(ZnS)��Ksp(CuS)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ձ�A��ʢ��0.1 mol/L��H2SO4��Һ���ձ�B��ʢ��0.1 mol/L��CuCl2��Һ(������Һ������)����ɵ�װ����ͼ��ʾ������˵������ȷ����(����)
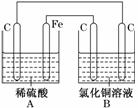
A��AΪԭ��أ�BΪ����
B��AΪ���أ�BΪԭ���
C����A�ձ��в���0.1 mol����ʱ��B�ձ��в�����������ʵ���ҲΪ0.1 mol
D������һ��ʱ�䣬B�ձ�����Һ��pH����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ͼ��ʾװ�ý���ʵ�飬���ش��������⣺
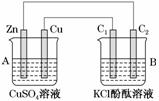 (1)�ж�װ�õ����ƣ�A��Ϊ________��B��Ϊ________________��
(1)�ж�װ�õ����ƣ�A��Ϊ________��B��Ϊ________________��
(2)п��Ϊ________�����缫��ӦʽΪ__________________��
ͭ��Ϊ________�����缫��ӦʽΪ________________________________________
________________________________________________________________________��
ʯī��C1Ϊ____�����缫��ӦʽΪ______________________________________
________________________________________________________________________��
ʯī��C2����������ʵ������Ϊ________________________________________
________________________________________________________________________��
(3)��C2������224 mL����(��״��)ʱ��п������________(����ӡ����١�)________g��CuSO4��Һ������________(����ӡ����١�)________g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪�����·�Ӧ����NH3��H��NH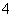 (ƽ�ⳣ��ΪK1)����Ag����Cl��AgCl(ƽ�ⳣ��ΪK2)����Ag����2NH3Ag(NH3)
(ƽ�ⳣ��ΪK1)����Ag����Cl��AgCl(ƽ�ⳣ��ΪK2)����Ag����2NH3Ag(NH3)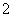 (ƽ�ⳣ��ΪK3)���١��ڡ��۵�ƽ�ⳣ����ϵΪK1>K3>K2���ݴ������������Ʋ��������(����)
(ƽ�ⳣ��ΪK3)���١��ڡ��۵�ƽ�ⳣ����ϵΪK1>K3>K2���ݴ������������Ʋ��������(����)
A���Ȼ��������ڰ�ˮ
B��������Һ�м��������Ȼ����а�ɫ����
C��������Һ�м��������а�ɫ����
D��������Һ���������������ȶ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���е��뷽��ʽ�У�������ǣ���
| A�� | H2CO3⇌H++HCO3����HCO3��⇌H++CO32�� | |
| B�� | H2SO4⇌2H++SO42�� | |
| C�� | NaHCO3�TNa++H++CO32�� | |
| D�� | NaHSO4�TNa++H++SO42�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com