
| A. | AgCl、AgBr、AgI均是难溶于水的固体,且要避光保存于棕色瓶中 | |
| B. | AgCl是白色难溶于水的固体,用于指纹鉴定有助于警察破案 | |
| C. | AgBr是黑色光敏性物质,常用于制作胶卷和人工降雨 | |
| D. | AgI是黄色固体,见光容易分解为单质碘和黑色的单质银,还常用于人工降雨 |
分析 A.AgCl、AgBr、AgI都是难溶于水的固体,都具有感光性;
B.利用留下的指纹中的氯化钠和硝酸银反应生成不溶于水和酸的氯化银白色沉淀比对指纹破案;
C.AgBr是淡黄色光敏性物质,AgBr不易形成结晶核;
D.AgI是黄色固体,见光分解,AgI有利于形成晶核,使水凝结;
解答 解:A.AgCl、AgBr、AgI均是难溶于水的固体,具有感光性见光易分解,要避光保存于棕色瓶中,故A正确;
B.指纹中的氯化钠和硝酸银反应生成不溶于水和酸的氯化银白色沉淀,用于指纹鉴定有助于警察破案,故B正确;
C.AgBr是淡黄色光敏性物质,常用作感光材料制作胶卷,AgBr不易形成结晶核不能用于人工降雨,故C错误;
D.AgI是黄色固体,见光容易分解为单质碘和黑色的单质银,AgI可在空气中形成结晶核,使水凝结,可用于人工降雨,故D正确;
故选C.
点评 本题考查学生卤素离子的还原性、单质的物理性质以及卤化银的溶解情况等,注意知识的归纳和梳理是关键,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ①②③ | C. | ①② | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2L1mol/LNaF溶液中含Na+和F-之和为4NA | |
| B. | 在常温常压下,22gCO2含有的共用电子对数为2NA | |
| C. | 7.1g氯气与足量的NaOH溶液反应,转移电子数为0.2NA | |
| D. | 11mol甲基(-CH3)中所含电子数为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应开始前,检查装置的气密性 | |
| B. | 加入过量稀硫酸,以确保镁带完全反应 | |
| C. | 反应停止后,立即调压并记录读数 | |
| D. | 常温下1mol氢气的体积为$\frac{V({H}_{2})}{m(Mg)}$×M(Mg) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯的加成反应和乙烯使酸性KMnO4溶液褪色,都与分子内含有的碳碳双键有关 | |
| B. | 相同质量的乙烯和甲烷完全燃烧后生成水的质量相同 | |
| C. | 乙烯的化学性质比乙烷活泼 | |
| D. | 用溴的四氯化碳溶液或酸性KMnO4溶液都可以鉴别乙烯和乙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性氧化物不一定都能与水反应生成酸 | |
| B. | 某溶液加入盐酸酸化的BaCl2溶液产生白色沉淀,则原溶液中含有SO42- | |
| C. | 丁达尔效应可以用于区别FeCl3溶液和Fe(OH)3胶体 | |
| D. | 现代化学分析测试常借助一些仪器来分析物质组成,如用原子吸收光谱确定物质中含有那些金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
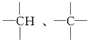 中的碳原子分别称为伯、仲、叔、季碳原子,数目分别用n1、n2、n3、n4表示,则烷烃(除甲烷外)中存在的关系有:(用以上符号回答)
中的碳原子分别称为伯、仲、叔、季碳原子,数目分别用n1、n2、n3、n4表示,则烷烃(除甲烷外)中存在的关系有:(用以上符号回答)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
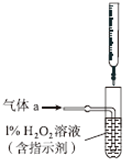 硫酸工业产生的废气(主要成分:SO2、O2、N2、CO2等)排放到空气中会污染环境.某化学兴趣小组对废气的组成进行探究,请回答下列问题:
硫酸工业产生的废气(主要成分:SO2、O2、N2、CO2等)排放到空气中会污染环境.某化学兴趣小组对废气的组成进行探究,请回答下列问题:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com