
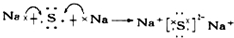 ��
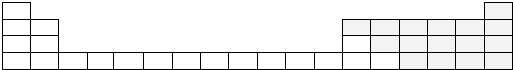
�� ���� ��1������ԭ�ӵ��Ӳ���������������ȷ�������ڱ��е�λ�ã�
��2����ԭ�Ӻ�����3�����Ӳ㣬����������Ϊ3���Դ�ȷ�������ڱ��е�λ�ã�
��3�����Ӳ���Խ�࣬ԭ�Ӱ뾶Խ���Ӳ�����ͬʱ��ԭ������Խ�뾶ԽС��
��4��Ԫ�صķǽ�����Խǿ��������������ˮ��������Խǿ����O��FԪ�س��⣻
��5����������������Һ��Ӧ����ƫ�����ƺ�������
��6������Ϊ���ӻ����
��� �⣺��1��OԪ��λ�ڵڶ����ڵ�VIA�塢NaԪ��λ�ڵ������ڵ�IA�塢AlԪ��λ�ڵ������ڵ�IIIA�塢SԪ��λ�ڵ������ڵ�VIA�塢ClԪ��λ�ڵ������ڵ�VIIA�壬�����������ڱ��е�λ��Ϊ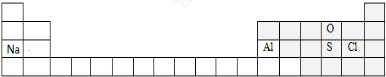 ��
��
�ʴ�Ϊ�� ��
��
��2����ԭ�Ӻ�����3�����Ӳ㣬����������Ϊ3����λ�����ڱ��������ڢ�A�壬�ʴ�Ϊ���������ڢ�A�壻
��3�����Ӳ���Խ�࣬ԭ�Ӱ뾶Խ���Ӳ�����ͬʱ��ԭ������Խ�뾶ԽС����ԭ�Ӱ뾶�Ӵ�С��ϵΪ��Na��Al��S��Cl��O��
�ʴ�Ϊ��Na��Al��S��Cl��O��
��4���صķǽ�����Խǿ��������������ˮ��������Խǿ����O��FԪ�س��⣬����OԪ��Ϊ���ǽ�������ǿ��Ԫ����ClԪ�أ���������ǿ������HClO4��
�ʴ�Ϊ��HClO4��
��5����������������Һ��Ӧ����ƫ�����ƺ���������Ӧ�����ӷ���ʽΪ2Al+2OH-+2H2O=2AlO2-+3H2�����ʴ�Ϊ��2Al+2OH-+2H2O=2AlO2-+3H2����
��6������Ϊ���ӻ�����õ���ʽ��ʾ�γɹ���Ϊ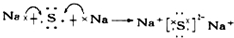 ���ʴ�Ϊ��
���ʴ�Ϊ��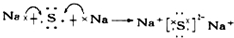 ��
��
���� ���⿼��Ԫ�����ڱ���Ԫ�������ɵ��ۺ�Ӧ�ã��漰Ԫ��������֪ʶ��ԭ�ӽṹʾ��ͼ��Ԫ�������ڱ��е�λ��ȷ����֪ʶ�㣬��ϤԪ�����ڱ��ṹ��ԭ�ӽṹ���ɽ��ע�����ԭ�Ӱ뾶��С�ıȽϷ�����


 ��ѧʵ����ϵ�д�
��ѧʵ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ԭ��Ӧ | B�� | ������Ӧ | C�� | �Ӿ۷�Ӧ | D�� | ��ȥ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ������ ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
| 2 | �� | �� | ||||||
| 3 | �� | �� | �� | �� | �� | �� | �� | |
| 4 | �� | ⑪ | ⑫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | CH3Br | B�� | CH3CH2CH2CH2Br | ||
| C�� | CH2BrCH2Br | D�� | CH2BrCH2CH2CH2Br |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��ͼ��ʾװ�ã�c��d������ʯī�缫���ش��������⣺
��ͼ��ʾװ�ã�c��d������ʯī�缫���ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| MnO2 | �����Թ���� | �۲��� | ��Ӧ��������ʱ�� |
| ��ĩ״ | ���� | ���ҷ�Ӧ�������ǵ�ľ����ȼ | 3.5min |
| ��״ | �� | ��Ӧ���������Ǻ�����ľ��δ��ȼ | 30min |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com