
 ij̽��С�������ͼ��ʾװ�ã��г֡����������ԣ���ģ�ҵ���������Ʊ�������ȩ��CCl3CHO����ʵ�飮�������ϣ��й���Ϣ���£�
ij̽��С�������ͼ��ʾװ�ã��г֡����������ԣ���ģ�ҵ���������Ʊ�������ȩ��CCl3CHO����ʵ�飮�������ϣ��й���Ϣ���£�| C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl | |
| �۵�/�� | -1 14.1 | -57.5 | 58 | -138.7 |
| �е�/�� | 78.3 | 97.8 | 198 | 12.3 |
| �ܽ��� | ��ˮ���� | ������ˮ���Ҵ� | ������ˮ���Ҵ� | ����ˮ���������Ҵ� |
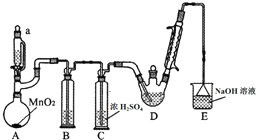
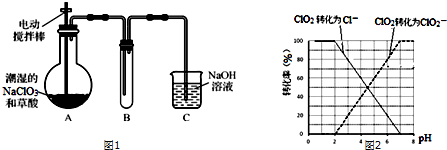
���� Aװ�����ö���������Ũ�����Ʊ�������Bװ���ñ���ʳ��ˮ��ȥHCl��Cװ��ʢ��Ũ�������������D�з�Ӧ�Ʊ�CCl3CHO��Eװ��ʢ������������Һ������β����������HCl��ֹ��Ⱦ������
��1������������Ũ�����ڼ��������·�Ӧ�����Ȼ��̡�������ˮ���ñ���ʳ��ˮ��ȥHCl��
��2����������ˮ��Ӧ����HCl��HClO���ᷢ����CCl3CHO+HClO��CCl3COOH���������ᣩ+HCl��C2H5OH+HCl��C2H5Cl+H2O�����Ʒ�Ӧ�¶���70�����ң�Ӧ��ȡˮԡ���ȣ�
��3��CCl3COOH�����Ҵ���CCl3CHO�������¶�ͨ��������룬��������װ��ѡ����Ҫ��������
��4���������ĵ�Na2S2O3����ʣ��I2�����ʵ���������������HCOO-��Ӧ��I2�����ʵ������ٸ��ݹ�ϵʽ��CCl3CHO��HCOO-��I2���㣻
��5������Խǿ������̶�Խ����ҺpHԽС��
��� �⣺Aװ�����ö���������Ũ�����Ʊ�������Bװ���ñ���ʳ��ˮ��ȥHCl��Cװ��ʢ��Ũ�������������D�з�Ӧ�Ʊ�CCl4CHO��Eװ��ʢ������������Һ������β����������HCl��ֹ��Ⱦ������
��1������������Ũ�����ڼ��������·�Ӧ�����Ȼ��̡�������ˮ����Ӧ����ʽΪ��MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O����������a��ʢ�ŵ��Լ���Ũ���ᣬBװ���ñ���ʳ��ˮ��ȥ�����е��Ȼ��⣬E���������ն����������Ȼ��⣬
�ʴ�Ϊ������ʳ��ˮ�����ն����������Ȼ��⣻
��2����������ˮ��Ӧ����HCl��HClO���ᷢ����CCl3CHO+HClO��CCl3COOH���������ᣩ+HCl��C2H5OH+HCl��C2H5Cl+H2O������װ��D�и����CCl3COOH��C2H5Cl���࣬���Ʒ�Ӧ�¶���70�����ң�Ӧ��ȡˮԡ���ȣ����Ⱦ��ȣ�ƫ�ڿ����¶ȣ�
�ʴ�Ϊ��CCl3COOH��C2H5Cl��ˮԡ��
��3��CCl3COOH�����Ҵ���CCl3CHO��Ӧ��ȡ�������з��룬���ƾ��ơ���Һ�ܡ��¶ȼơ���ƿ�⣬���貣��������������ƿ�������ܣ�
�ʴ�Ϊ������ ������ƿ�������ܣ�
��4���������ĵ�Na2S2O3����
ʣ��I2�����ʵ���0.02000mol•L-1��0.02L=2��10-4mol����HCOO-��Ӧ��I2�����ʵ���Ϊ0.1000mol•L-1��0.02L-2��10-4mol=1.8��10-3mol����CCl3CHO��HCOO-��I2��֪��CCl3CHO�����ʵ���Ϊ1.8��10-3mol�����Ʒ�Ĵ���Ϊ$\frac{1.8��1{0}^{-3}mol��147.5g/mol}{0.3g}$��100%=88.5%��
�ʴ�Ϊ��88.5%��
��5���ֱ�ⶨ0.1mol•L-1��������Һ��pH�����������pH��С��˵�������������̶ȱ�����Ĵ���������������Ա������ǿ��
�ʴ�Ϊ���ֱ�ⶨ0.1mol•L-1��������Һ��pH�����������pH��С��˵�������������Ա������ǿ��
���� ���⿼���л����Ʊ������ʺ����̶ȡ�ʵ�鷽����Ƶȣ��ؼ�����ȷ��Ӧԭ�����װ�����ã����ճ������ʷ����ᴿ������ע�����Ŀ��Ϣ��Ӧ�ã���Ŀ�Ѷ��еȣ������ڿ���ѧ����ʵ��̽�������ͼ���������


 ��ɢ˼ά�¿���ϵ�д�
��ɢ˼ά�¿���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ȳ��ǵ����Ҳ���Ƿǵ���� | |
| B�� | ����ȼ�յIJ���ɵ������� | |
| C�� | ���������ȼ�ϵ�ص�ȼ�� | |
| D�� | �������IJ�ͬ������ȫȼ�գ�����ĺ��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
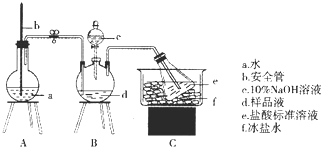
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
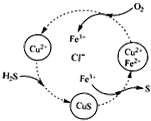 �ú�FeCl3��FeCl2��CuCl2�Ļ����Һ�Ϳ���������H2S������S������ʵ�ֻ���Һ��ѭ����������ת����ϵ��ͼ�������й�˵��������ǣ�������
�ú�FeCl3��FeCl2��CuCl2�Ļ����Һ�Ϳ���������H2S������S������ʵ�ֻ���Һ��ѭ����������ת����ϵ��ͼ�������й�˵��������ǣ�������| A�� | �⡢�ȡ�ͭ��Ԫ�صĻ��ϼ�δ�����ı� | |
| B�� | ת�������а���������ѧ��Ӧ | |
| C�� | ת�������л�ԭ��ΪH2S��FeCl2 | |
| D�� | �ܷ�Ӧ�ɱ�ʾΪ��2H2S+O2��2S+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����п����й������ | B�� | ������Һ�д���Fe2+��Fe3+��Cu2+ | ||
| C�� | ԭ������n��Fe2O3����n��Cu�� | D�� | �ټ���ͭ����Һ��ɫ����ȥ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����β�����ŷ����������ЧӦ����Ҫԭ�� | |
| B�� | ��������������Ԫ�أ���ʳ�ù���Ҳ������� | |
| C�� | ��ά���������ڿ�ˮ��������ǣ���������֯��Ӫ����Ҫ | |
| D�� | �����dz��õ�ˮ�������������ڳ�������ˮ��ɱ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���� HCl��H2SO3 | B�� | ������ Mg��Al | C�� | ���� NaOH��Mg��OH��2 | D�� | �ȶ��� HF��HCl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ľ�Ǵ�����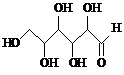 �����������ǣ� �����������ǣ� ��������Ϊͬϵ��� ��������Ϊͬϵ����������� | |
| B�� | ����ʽΪC6H14���л�����һ�ȴ��������֣����л��������3��3-�������� | |
| C�� | ����ϩ��PE���;�����ϩ��PVC���ĵ��嶼�Dz�������������ʹ��ˮ��ɫ | |
| D�� | ����������ϩ�����ѡ�̼���������CH3OCOOCH3����ȫȼ�պ�����һ������ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com