
 实验探究是学习化学的一个重要方法,某实验小组的同学利用下列装置完成一些常见气体制备以及相关物质性质探究(夹持装置及连接橡胶管已省略,其中装置E有多个供使用).
实验探究是学习化学的一个重要方法,某实验小组的同学利用下列装置完成一些常见气体制备以及相关物质性质探究(夹持装置及连接橡胶管已省略,其中装置E有多个供使用).| 液体试剂 | 固体药品 |
| 稀硫酸、稀盐酸、稀硝酸、NaOH溶液、浓氨水、5%H2O2溶液、浓盐酸、饱和食盐水 | CaCO3、CaO、MnO2、KMnO4、 碱石灰、Cu、Zn、Na2S |
分析 (1)要得到纯净干燥的氨气需将氨气通过盛有碱石灰的D装置,要得到纯净干燥的氯气需依次通过饱和食盐水和浓硫酸,故仪器的连接顺序是A→D→C←E←E←B;
(2)D装置的目的是干燥氨气,故需将氨气通过盛有碱石灰,要得到纯净干燥的氯气需依次通过饱和食盐水和浓硫酸,除去氯化氢和水分;
(3)根据已知信息判断出生成物,然后配平的反应的化学方程式为3Cl2+8NH3=6NH4Cl+N2;
(4)根据氯化铵电离出铵根离子和氯离子的特性进行检验.
解答 解:(1)要得到纯净干燥的氨气需将氨气通过盛有碱石灰的D装置,要得到纯净干燥的氯气需依次通过饱和食盐水和浓硫酸,故仪器的连接顺序是A→D→C←E←E←B,
故答案为:D;E;E;
(2)D装置的目的是干燥氨气,故需将氨气通过盛有碱石灰;要得到纯净干燥的氯气需依次通过饱和食盐水和浓硫酸,除去氯化氢和水分,
故答案为:e;c、f;
(3)C内出现大量白烟应为氯化铵固体,另一种生成物常用作食品包装袋内的保护气的气体为氮气,反应的化学方程式为:3Cl2+8NH3=6NH4Cl+N2,
故答案为:3Cl2+8NH3=6NH4Cl+N2;
(4)C内出现大量白烟应为氯化铵固体,氯化铵可电离出铵根离子和氯离子,检验白烟物质中的离子的实验方案为:将白烟配成水溶液取适量于试管中,先用硝酸酸化,加入硝酸银有白色沉淀说明有Cl-,再取一份加入过量氢氧化钠,加热产生有刺激性气味气体,能使湿润的红色石蕊试纸变蓝说明有NH4+,
故答案为:将白烟配成水溶液取适量于试管中,先用硝酸酸化,加入硝酸银有白色沉淀说明有Cl-,再取一份加入过量氢氧化钠,加热产生有刺激性气味气体,能使湿润的红色石蕊试纸变蓝说明有NH4+.
点评 本题考查实验方案的设计,题目难度中等,熟悉氨气的制取、氯气的制取原理及物质的性质是解答本题的关键,注意发生的氧化还原反应为解答的难点,试题培养了学生的分析能力及化学实验能力.


科目:高中化学 来源: 题型:选择题
| A. | 向AlCl3溶液中滴加过量氨水:Al3++3OH-═Al(OH)3↓ | |
| B. | 向NaNO2溶液中滴加酸性KMnO4溶液:5NO2-+2MnO4-+3H2O═5NO3-+2Mn2++6OH- | |
| C. | 醋酸除去水垢中的CaCO3:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | 向偏铝酸钠溶液中通入过量的CO2:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A、B、C、D、E、F六种元素的原子序数依次增大,A的最高价和最低价的绝对值相等,B的基态原子有3个不同的能级且各能级中电子数相等,D的基态原子与B的基态原子未成对电子数目相同,E的基态原子s能级的电子总数与p能级的电子数相等,F的基态原子的3d轨道是4s电子数的4倍.请回答下列问题:
A、B、C、D、E、F六种元素的原子序数依次增大,A的最高价和最低价的绝对值相等,B的基态原子有3个不同的能级且各能级中电子数相等,D的基态原子与B的基态原子未成对电子数目相同,E的基态原子s能级的电子总数与p能级的电子数相等,F的基态原子的3d轨道是4s电子数的4倍.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含等物质的量的AlO2-、OH-、CO32-的溶液中,逐滴加入盐酸:AlO2-、OH-、CO32- | |
| B. | 含等物质的量的Fe3+、Cu2+、H+的溶液中加入锌粉:Fe3+、Cu2+、H+、Fe2+ | |
| C. | 含等物质的量的Ba(OH)2、KOH的溶液中,缓慢通入CO2:KOH、Ba(OH)2、K2CO3、BaCO3 | |
| D. | 含等物质的量的FeBr2、FeI2的溶液中,缓慢通入氯气:I-、Br-、Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
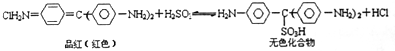
| A. | 品红溶液中同时通入Cl2、SO2,漂白效果会更好 | |
| B. | 加热可判断品红褪色是通入SO2还是通入Cl2引起的 | |
| C. | “无色化合物”分子中,19个碳原子都可能在同一平面上 | |
| D. | 无色化合物中的官能团有苯环、磺酸基、氨基 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 砷的外围电子排布式:3d104S24p3 | |
| B. | 质子数为35、中子数为45的溴原子:${\;}_{35}^{80}$Br | |
| C. | 硫离子的结构示意图: | |
| D. | 过氧化钠的电子式: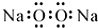 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com