
设N A为阿伏加德罗常数的值,下列叙述正确的是
A.60gSiO 2晶体有σ键4N A
B.在标准状况下,2.24 LSO3中含有的氧原子数为0.3NA
C.t℃时,MgCO3的 Ksp=4×10-6,则饱和溶液中含 Mg2+数目为2×10-3NA
D.标准状况下,2.24LCl2通入足量H2O溶液中转移的电子数为0.1NA
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源:2015-2016学年海南嘉积中学高二下期中理科化学试卷(解析版) 题型:选择题
某烃结构式如下: -C≡C-CH=CH-CH3,有关其结构说法正确的是
-C≡C-CH=CH-CH3,有关其结构说法正确的是
A.所有原子可能在同一平面上 B.所有原子可能在同一条直线上
C.所有碳原子可能在同一平面上 D.所有氢原子可能在同一平面上
查看答案和解析>>
科目:高中化学 来源:2016届宁夏银川二中高三三模理综化学试卷(解析版) 题型:选择题
山梨酸是一种食品添加剂的成分,其结构如图所示,下列说法正确的是
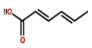
A.该有机物与等物质的量Br2发生加成反应时,可生成两种加成产物
B.该有机物能与金属Na、NaOH溶液、Na2CO3溶液、NaHCO3溶液发生反应
C.该有机物能发生加成、取代、氧化、消去、加聚反应
D.可使用酸性高锰酸钾溶液鉴别该有机物和乳酸(2-羟基丙酸)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川成都石室中学高二4月月考化学试卷(解析版) 题型:选择题
关于电化学的下列说法正确的是

A.工业上用电解MgCl2溶液的方法冶炼Mg
B.钢铁发生吸氧腐蚀的正极反应式为4OH﹣-4e﹣═O2↑+2H2O
C.如图14-C中发生反应的方程式为:Fe+2H+=Fe2++H2↑
D.碱性锌锰干电池放电时的正极反应为: MnO2+H2O+e-=MnOOH+OH-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川成都石室中学高二4月月考化学试卷(解析版) 题型:选择题
某烃的结构简式为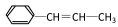 ,它可能具有的性质是
,它可能具有的性质是
A.可以发生加成、取代、氧化反应
B.能使溴水褪色,但不能使酸性高锰酸钾褪色
C.能发生加聚反应,其生成物可用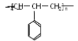 来表示
来表示
D.易溶于水,也易溶于有机溶剂
查看答案和解析>>
科目:高中化学 来源:2016届宁夏石嘴山三中高三下四模理综化学试卷(解析版) 题型:填空题
二氧化氯(ClO2)是国内外公认的高效、广谱、快速、安全无毒的杀菌消毒剂,被称为“第4代消毒剂”。工业上可采用氯酸钠(NaClO3)或亚氯酸钠(NaClO2)为原料制备ClO2。
(1)亚氯酸钠也是一种性能优良的漂白剂,但在强酸性溶液中会发生歧化反应,产生ClO2气体,离子方程式为___________________________;向亚氯酸钠溶液中加入盐酸,反应剧烈。若将盐酸改为相同pH的硫酸,开始时反应缓慢,稍后一段时间产生气体速率迅速加快。产生气体速率迅速加快的原因是 。
(2)化学法可采用盐酸或双氧水还原氯酸钠制备ClO2。用H2O2作还原剂制备的ClO2更适合用于饮用水的消毒,其主要原因是 。
(3)电解法是目前研究最为热门的生产ClO2的方法之一。如图所示为直接电解氯酸钠、自动催化循环制备高纯ClO2的实验。
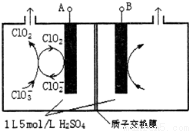
①电源负极为___________________极(填A或B)
②写出阴极室发生反应的电极反应式和离子方程式
_______________________ ___ ; 。
③控制电解液H+不低于5mol/L,可有效防止因H+浓度降低而导致的ClO2—歧化反应。若两极共收集到气体22.4L(体积已折算为标准状况,忽略电解液体积的变化和ClO2气体溶解的部分),此时阳极室与阴极室c(H+)之差为_________________。
查看答案和解析>>
科目:高中化学 来源:2016届宁夏石嘴山三中高三下四模理综化学试卷(解析版) 题型:选择题
短周期元素R、T、X、Y、Z在元素周期表的相对位置如下表所示,它们的最外层电子数
之和为24。则下列判断正确的是
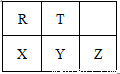
A.气态氢化物稳定性:Y>T
B.R能分别与X、Z形成共价化合物
C.R位于元素周期表中第二周期第VA族
D.Z元素的最高价氧化物对应的水化物的化学式为HZO4
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省高三第七次模拟理综化学试卷(解析版) 题型:填空题
[化学—选修3:物质结构与性质]
(1)下列有关微粒间作用力的说法正确的是
A.配位键的强度有大有小,所以有的配合物很稳定,有的很不稳定
B.水加热到很高的温度都难以分解是因为水分子间存在氢键
C.壁虎能在光滑的墙壁上行走是因为壁虎脚底的细毛与物体表面的分子产生分子间作用力
D.互为手性异构本的分子具有完全相同的组成和原子排列,所以生产手性药物时无需分离手性异构体
(2)判断下列哪个模型代表金属晶体锌的堆积方式 。

(3)第四周期未成对电子数最多的P区元素的元素符号是 ,核外电子占据
个原子轨道。
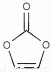
(4)碳酸亚乙烯酯是锂离子电池低温电解液的重要添加剂,其结构如图。碳原子的杂化方式有 ,分子中σ键与π键之比为 。
(5)比较NH2-和NH3的键角∠HNH的大小:NH2- NH3(填“﹥”“=”“﹤”),请用价层电子对互斥规解释: 。
(6)SO32-中硫原子的价层电子对互斥模型是 ;写出一种与SO32-互为等电子体的分子 。
(7)SiC晶胞与金刚石晶胞相似,设晶胞边长为a cm,碳原子直径为b cm,硅原子直径为c cm,则该晶胞的空间利用率为 。
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三第九次月考化学试卷(解析版) 题型:选择题
设NA为阿佛加德罗常数.下列说法正确的是
A.lmol羟基和lmol氢氧根离子所含的电子数均为10NA
B.0.lmol/L乙酸溶液中所含醋酸根离子的数目小于0.1NA
C.当合成氨反应达到平衡时,表明每生成6NA个N-H键的同时必生成3NA个H-H键
D.46g由NO2和N2O4组成的混合气体中所含的原子数为3NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com