
【题目】Ⅰ.(1)①H2 + CuO ![]() Cu + H2O
Cu + H2O
②CaCO3 + 2HCl = CaCl2 + CO2↑ + H2O
③3S + 6NaOH ![]() 2Na2S + Na2SO3 + 3H2O
2Na2S + Na2SO3 + 3H2O
④NH4NO3 + Zn = ZnO + N2↑+ 2H2O
⑤Cu2O + 4HCl = 2HCuCl2 + H2O
上述反应中,属于氧化还原反应的是__________________________(填序号)
(2)SeO2、KI和HNO3可发生反应:SeO2+KI+HNO3→Se+I2+KNO3+H2O,配平该反应的化学方程式并用双线桥法标出电子转移的方向和数目:____________________________。
(3)在反应 KIO3 + 6HI = 3I2 + KI + 3H2O中,氧化剂与还原剂的物质的量之比为__________。
Ⅱ.已知:
① 2H2O + Cl2 + SO2 = H2SO4 + 2HCl ② 2KMnO4 + 16HCl = 2KCl + 2MnCl2 + 5Cl2↑ + 8H2O
(4)根据以上两个反应可以得出氧化剂和还原剂的强弱顺序,请写出由KMnO4、K2SO4 、MnSO4 、SO2、H2O、H2SO4 这六种物质组成的氧化还原反应的方程式并配平:_______________________。
在反应②中,若有18.25g HCl被氧化,求:
(5)转移的电子数为:_______________。
(6)标况下生成Cl2的体积(请列式计算)_______。
【答案】①③④ 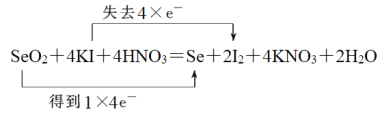 1:5 2KMnO4+5SO2+2H2O=K2SO4+2MnSO4+2H2SO4 0.5NA或3.01×1023 5.6L
1:5 2KMnO4+5SO2+2H2O=K2SO4+2MnSO4+2H2SO4 0.5NA或3.01×1023 5.6L
【解析】
Ⅰ.(1)反应前后有元素化合价升降的反应是氧化还原反应,据此判断。
(2)根据反应中元素的化合价变化情况,结合电子得失守恒解答。
(3)根据反应中元素的化合价变化情况,结合电子得失守恒解答。
Ⅱ.根据氧化还原反应中氧化剂的氧化性强于氧化产物的氧化性,还原剂的还原性强于还原产物的还原性,判断出氧化性、还原性强弱,根据氧化还原反应规律书写方程式,结合方程式和元素的化合价变化计算。
(1)①反应H2 + CuO ![]() Cu + H2O中H元素化合价升高,Cu元素化合价降低,属于氧化还原反应;
Cu + H2O中H元素化合价升高,Cu元素化合价降低,属于氧化还原反应;
②反应CaCO3 + 2HCl=CaCl2 + CO2↑ + H2O中元素的化合价均没有发生变化,不是氧化还原反应;
③反应3S + 6NaOH ![]() 2Na2S + Na2SO3 + 3H2O中S元素的化合价部分升高,部分降低,属于氧化还原反应;
2Na2S + Na2SO3 + 3H2O中S元素的化合价部分升高,部分降低,属于氧化还原反应;
④反应NH4NO3 + Zn=ZnO + N2↑+ 2H2O中Zn元素化合价升高,铵根中N元素化合价升高,硝酸根中N元素化合价降低,属于氧化还原反应;
⑤反应Cu2O + 4HCl=2HCuCl2 + H2O中元素的化合价均没有发生变化,不是氧化还原反应;
则上述反应中,属于氧化还原反应的是①③④;
(2)反应中Se元素化合价从+4价降低到0价得到4个电子,I元素化合价从-1价升高到0价,失去1个电子,根据电子得失守恒可知转移电子是4个,因此配平该反应的化学方程式并用双线桥法标出电子转移的方向和数目为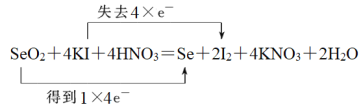 。
。
(3)在反应KIO3 + 6HI=3I2 + KI + 3H2O中碘酸钾中碘元素化合价从+5价降低到0价,得到5个电子,碘酸钾是氧化剂,HI中碘元素化合价从-1价升高到0价,失去1个电子,HI是还原剂,根据电子得失守恒可知氧化剂与还原剂的物质的量之比为1:5。
Ⅱ.(4)①反应2H2O + Cl2 + SO2=H2SO4 + 2HCl中氯气是氧化剂,二氧化硫是还原剂,硫酸是氧化产物,所以氧化性是Cl2>H2SO4;②反应2KMnO4 + 16HCl=2KCl + 2MnCl2 + 5Cl2↑ + 8H2O中高锰酸钾是氧化剂,氯化氢是还原剂,氯气是氧化产物,所以氧化性是KMnO4>Cl2↑,因此由KMnO4、K2SO4、MnSO4、SO2、H2O、H2SO4这六种物质组成的氧化还原反应中氧化剂是高锰酸钾,二氧化硫是还原剂,则反应的方程式为2KMnO4+5SO2+2H2O=K2SO4+2MnSO4+2H2SO4。
(5)在反应②中,若有18.25g HCl被氧化,即被氧化的氯化氢的物质的量是18.25g÷36.5g/mol=0.5mol。反应中氯元素化合价从-1价升高到0价,则转移电子的物质的量是0.5mol×1=0.5mol,电子数为0.5NA。
(6)根据氯原子守恒可知生成氯气是0.5mol÷2=0.25mol,在标况下的体积为0.25mol×22.4L/mol=5.6L。


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
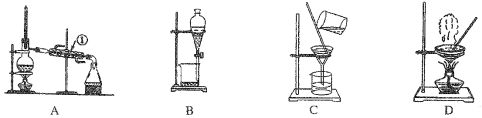
(1)从氯化钾溶液中得到氯化钾固体,选择装置___________(填代表装置图的字母,下同);除去自来水中的C1-等杂质,选择装置_____________。
(2)从碘水中分离出I2,选择装置__________,该分离方法的名称为__________________。
(3)装置A中①的名称是______________,进水的方向是从__________(填“上”或“下” )口进水。装置B在分液时为使液体顺利流下,先进行的操作是________________________________,后再打开下端活塞。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下可将煤转化为水煤气,水煤气可作为气体燃料,有关热化学方程式如下:
①C(s)+H2O(g)=CO(g)+H2(g) ΔH1=+131.3 kJ/mol
②2CO(g)+O2(g)=2CO2(g) ΔH2=-566.0 kJ/mol
③2H2(g)+O2(g)=2H2O(g) ΔH3=-483.6 kJ/mol
下列说法正确的是
A. 煤不属于化石燃料
B. 等质量的CO和H2完全燃烧时,前者放热多
C. 水煤气作为气体燃料,比煤直接燃烧污染小
D. 由反应③可以确定H2的燃烧热为241.8 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在无色酸性溶液中可以大量共存的有( )
A.Ag+、K+、NO3﹣、Cl ﹣
B.K+、Cu2+、SO42﹣、HCO3﹣
C.Mg2+、Cl﹣、SO42﹣、Na+
D.CO32﹣、K+、NO3﹣、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述的化学用语中,正确的是
A. 用石墨作电极电解AlCl3溶液:2Cl-+2H2O![]() Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
B. 在高温氧化锆的环境下,CO的燃料电池的负极反应2CO+2O2--4e-=2CO2
C. 硫化钠的水解方程式:S2-+2H2O![]() H2S+2OH-
H2S+2OH-
D. 电解硫酸钠水溶液的阳极反应:2H++2e-=H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关蛋白质的叙述中,不正确的是
A. 蛋白质水解的最终产物为氨基酸
B. 酒精消毒的原理是让细菌蛋白质变性死亡
C. 向蛋白质溶液中加入饱和硫酸铵溶液,有沉淀析出,再加入水沉淀不溶解
D. 浓硝酸溅在皮肤上,使皮肤呈黄色,是由于浓硝酸和蛋白质发生显色反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极都为情性电极。测得同温同压下,气体甲与气体乙的体比约为1: 2,以下说法正确的是
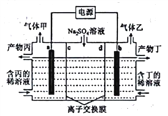
A. a极与电源的负极相连 B. 离子交换膜d为阴离子交换膜
C. 产物丙为硫酸溶液 D. 每转移0.2mol e- 则产生1.12L气体乙(标况下)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将质量均为m g的O2、X、Y气体分别充入相同容积的密闭容器中,压强(P)与温度(T)的关系如图所示,则X、Y气体可能分别是( )
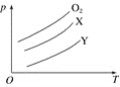
A. C2H4、CH4 B. CO2、Cl2
C. SO2、CO2 D. CH4、Cl2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com