
| A、所用NaOH已经潮解 |
| B、定容时仰视刻度线 |
| C、有少量NaOH溶液残留在烧杯里 |
| D、称量时所用砝码生锈 |
科目:高中化学 来源: 题型:
| A、②<①<③=④ |
| B、①=②=③=④ |
| C、①<②<③<④ |
| D、②<③<①<④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
3 2 |
3 2 |
4 2 |
A、
| ||||
B、
| ||||
C、
| ||||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| 容器 编号 | 起始时各物质物质的量/mol | 达到平衡的时间 | 达平衡时体系能量的变化 | ||
| X2 | Y2 | XY3 | |||
| ① | 1 | 3 | 0 | 2分钟 | 放热46.3kJ |
| ② | 0.4 | 1.2 | 1.2 | / | Q(Q>0) |
A、平衡时,容器②中X2的体积分数为
| ||
| B、平衡时,两个容器中XY3的物质的量浓度相等 | ||
C、容器①、②中反应的平衡常数相等,K=
| ||
| D、容器①体积为0.3L,则达平衡时放出的热量小于46.3kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
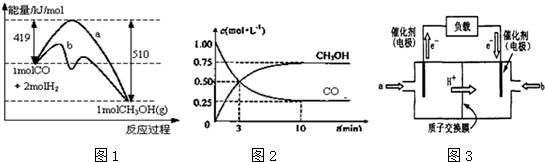
| 物质 | CO | H2 | CH3OH |
| 浓度/(mol?L-1) | 0.1 | 0.2 | 0.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
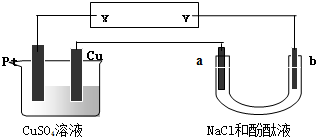
| A、NaCl溶液浓度不变 |
| B、X是负极,Y是正极 |
| C、CuSO4溶液浓度变小 |
| D、X是正极,Y是负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
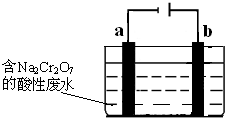
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验操作 | 实验现象 | 结论 | |
| A | 向硅酸钠溶液中滴加1滴酚酞,再逐滴加入稀盐酸至红色褪去 | 2 min后,试管里出现凝胶 | 酸性:盐酸>硅酸 |
| B | 在酒精灯上加热铝箔 | 铝箔熔化但不滴落 | 熔点:氧化铝>铝 |
| C | 常温下,向浓硫酸中投入铝片 | 铝片不溶解 | 常温下,铝不与浓硫酸反应 |
| D | 向某无色溶液中先滴加氯水,再加少量CCl4,振荡,静置 | 溶液分层,下层为橙红色 | 溶液中含有Br- |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com