
实验:①0.1 mol·L-1AgNO3溶液和0.1 mol·L-1NaCl溶液等体积混合得到浊液a,过滤得到滤液b和白色沉淀c;
②向滤液b中滴加0.1 mol·L-1KI溶液,出现浑浊;
③向沉淀c中滴加0.1 mol·L-1KI溶液,沉淀变为黄色。
下列分析不正确的是
A.浊液a中存在沉淀溶解平衡:AgCl(s)  Ag+(aq)+Cl-(aq)
Ag+(aq)+Cl-(aq)
B.滤液b中不含有Ag+
C.③中颜色变化说明AgCl转化为AgI
D.实验可以证明AgI比AgCl更难溶
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014高考名师推荐化学环境污染与保护(解析版) 题型:选择题
有关海洋中部分资源的利用的说法不正确的是
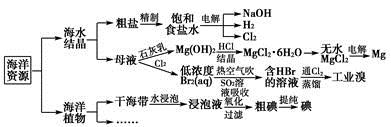
A.工业上利用Cl2与澄清石灰水反应制取漂白粉
B.用MgCl2·6H2O晶体制无水MgCl2,需在HCl气流中加热脱水
C.SO2水溶液吸收Br2的化学方程式为Br2+SO2+2H2O=H2SO4+2HBr
D.粗碘中混有少量ICl和IBr可加入KI进行升华提纯
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学燃烧热与盖斯定律(解析版) 题型:选择题
某一化学反应在不同条件下的能量变化曲线如右图所示。下列说法正确的是
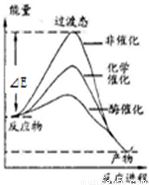
A.化学催化比酶催化的效果好
B.使用不同催化剂可以改变反应的热效应
C.使用不同催化剂可以改变反应的能耗
D.反应物的总能量低于生成物的总能量
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学热化学方程式的正误判断及书写(解析版) 题型:选择题
已知:①101 kPa时,2C(s)+O2(g)===2CO(g) ΔH=-221 kJ/mol;
②稀溶液中,H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ/mol。
下列结论正确的是
A.碳的燃烧热大于110.5 kJ/mol
B.①的反应热为221 kJ/mol
C.浓硫酸与稀NaOH溶液反应的中和热为-57.3 kJ/mol
D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学溶度积、沉淀的生成、溶解、转化(解析版) 题型:选择题
25 ℃时,5种银盐的溶度积常数(Ksp)分别是:
AgCl | Ag2SO4 | Ag2S | AgBr | AgI |
1.8×10-10 | 1.4×10-5 | 6.3×10-50 | 7.7×10-13 | 8.51×10-16 |
下列说法正确的是
A.氯化银、溴化银和碘化银的溶解度依次增大
B.将硫酸银溶解于水后,向其中加入少量硫化钠溶液,不可能得到黑色沉淀
C.在5 mL 1.8×10-5 mol·L-1的NaCl溶液中,加入1滴(1 mL约20滴)0.1 mol·L-1的AgNO3溶液,不能观察到白色沉淀
D.将浅黄色溴化银固体浸泡在饱和氯化钠溶液中,可以有少量白色固体生成
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学水的电离与溶液酸碱性(解析版) 题型:选择题
下列叙述不正确的是
A.向纯水中加入少量CH3COONa固体,促进了水的电离
B.25°C 时,pH=3的醋酸与pH=3的HCl对水的电离抑制作用相同
C.25°C时,pH=3的NH4Cl溶液中,水电离出的c(H+)是10-3mol/L
D.升高温度,纯水电离出的c(H+)增大,pH减少,显酸性
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学氮气、氧化物及硝酸(解析版) 题型:实验题
某化学兴趣小组为验证NO2的氧化性和NO的还原性,设计了如下装置制取NO2和NO,并验证其性质:
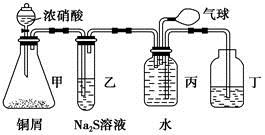
(1)写出甲中反应的离子方程式:_____________________
乙中的现象是__________________________________________________
可证明NO2的氧化性;在丙中鼓入空气后的现象是_____________________________________,可证明NO的还原性。
(2)实验前丙中充满水的作用是________________________________________
(用反应的化学方程式和简要文字回答)。
(3)小华对上述实验设计提出了质疑,他认为乙中的现象不足以证明NO2的氧化性,他的理由是_________________________________________________。
你认为怎样才能准确证明NO2的氧化性?___________________________
(简要回答出原理和现象即可)。
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学氧化还原反应方程式的配平及相关计算(解析版) 题型:填空题
(1)请将下列五种物质:KBr、Br2、I2、KI、K2SO4分别填入下列横线上,组成一个未配平的化学方程式:
KBrO3+ +H2SO4—→ + + + +H2O。
(2)如果该化学方程式中I2和KBr的化学计量数分别是8和1,则①Br2的化学计量数是 ;
②请将反应物的化学式及配平后的化学计量数填入下列相应的位置中:
KBrO3+ + H2SO4—→……;
③若转移10 mol电子,则反应后生成I2的物质的量为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com