
| A. | 使酚酞变红色的溶液:Na+、Cu2+、Fe2+、NO3- | |
| B. | 使PH试纸变红的溶液中:Na+、Mg2+、SO42-、NH4+ | |
| C. | c(H+)=0.1mol•L-1的溶液:Na+、NH4+、SO42-、F- | |
| D. | 与铁粉反应放出H2的无色溶液:Na+、Cl-、HCO3-、SO42- |
分析 A.使酚酞变红色的溶液中存在大量氢氧根离子,铜离子、亚铁离子与氢氧根离子反应;
B.使pH试纸变红的溶液中呈酸性,溶液中存在大量氢离子,四种离子之间不反应,都不与氢离子反应;
C.氟离子与氢离子反应生成氟化氢;
D.与铁粉反应放出H2的无色溶液呈酸性,碳酸氢根离子与氢离子反应.
解答 解:A.使酚酞变红色的溶液呈碱性,溶液中存在大量氢氧根离子,Cu2+、Fe2+与氢氧根离子反应,在溶液中不能大量共存,故A错误;
B.使PH试纸变红的溶液中存在大量氢离子,Na+、Mg2+、SO42-、NH4+之间不发生反应,都不与氢离子反应,在溶液中能够大量共存,故B正确;
C.F-与氢离子反应生成弱电解质HF,在溶液中不能大量共存,故C错误;
D.与铁粉反应放出H2的无色溶液中存在大量氢离子,HCO3-与氢离子反应,在溶液中不能大量共存,故D错误;
故选B.
点评 本题考查离子共存的判断,为高考的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:实验题
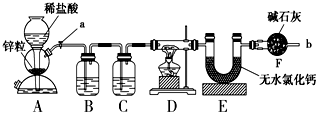
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 滴加AgNO3溶液,观察是否有白色沉淀 | |
| B. | 滴加AgNO3溶液、稀硝酸和NaNO2溶液,观察是否有白色沉淀 | |
| C. | 滴加NaOH溶液,并加热片刻,再用稀硝酸酸化后,滴入AgNO3溶液观察是否有白色沉 | |
| D. | 滴加AgNO3溶液和稀硝酸,观察是否有白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有泥沙的浑水,静置一会儿水沙分离,可取得上层的清水 | |
| B. | 农村“扬谷”分离饱满的谷粒和干瘪的谷壳 | |
| C. | 建筑工地上用铁筛把大小不同的沙粒分开 | |
| D. | 淘米除去米中混有的小沙粒 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 0.5mol N2中含有0.5NA个N | |
| B. | 32gO2中含有的氧原子数为2NA | |
| C. | H2的摩尔质量是为2 | |
| D. | 1molH2SO4在水溶液电离出离子约为1.806×1024个 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
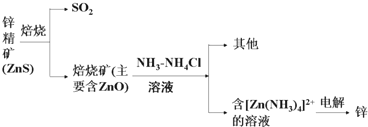
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
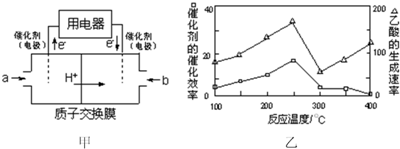
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 糖类、油脂、蛋白质都是高分子化合物,都能发生水解反应 | |
| B. | 淀粉、纤维素水解的最终产物均为葡萄糖 | |
| C. | 由甲烷的氯代物有4种,可推知乙烷的氯代物有6种 | |
| D. | 天然油脂没有固定的熔点和沸点,所以天然油脂是混合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com