
在2012年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X、Y为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1 molXY2含有54 mol电子。
(1)该融雪剂的化学式是 ;X与氢元素形成的化合物的电子式是 。
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是 ;D与E能形成一种非极性分子,该分子的结构式为 ;D所在族元素的氢化物中,沸点最低的是 。
(3)元素W与Y同周期,其单质是原子晶体;元素Z的单质分子Z2中有3个共价健;W与Z能形成一种新型无机非金属材料,其化学式是 .
(4)元素R与Y同主族,其氢化物能用于刻蚀玻璃,R2与NaOH溶液反应的产物之一是OR2,该反应的离子方程式为 。
科目:高中化学 来源: 题型:
已知(CH3)2C===CH2,可表示为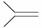 ,脱落酸(如图)可用作植物生长抑制剂,下列对该物质的叙述正确的是( )
,脱落酸(如图)可用作植物生长抑制剂,下列对该物质的叙述正确的是( )
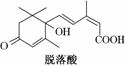
A.其分子式为C15H22O4
B.其属于芳香族化合物
C.1 mol该物质最多可与4 mol H2发生反应
D.该物质在一定条件下可发生自身取代反应生成含七元环的物质
查看答案和解析>>
科目:高中化学 来源: 题型:
A是一种可以作为药物的有机化合物。请从下列反应图式中各有机物的关系(所有无机物均已略去),回答下列问题:
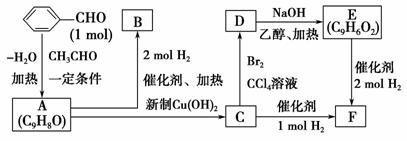
(1)推测有机物A、B、C、E、F的结构简式。
(2)写出下列反应的反应类型:CD: __________________________________;
DE: __________________________________________________________。
(3)写出下列反应的化学方程式:
AB: ____________________________________________________________;
AC: ____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
W、X、Y、Z均为短周期元素,W的最外层电子数与核外电子总数之比为7:17;X与W同主族;Y的原子序数是W和X的原子序数之和的一半;含Z元素的物质焰色反映为黄色。下列判断正确的是
A.金属性:Y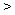 Z B 氢化物的沸点:
Z B 氢化物的沸点: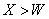
C.离子的还原性: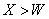 D 原子及离子半径:
D 原子及离子半径: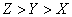
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素A、B、C的原子序数依次递增,它们的原子最外层电子数之和为12,A与C同主族,B原子的最外层电子数等于A原子的次外层电子数,则下列叙述正确的是
A.原子半径:A<B<C
B.A的氢化物稳定性大于C的氢化物稳定性
C.三种元素的最高价氧化物对应水化物均可由化合反应得到
D.高温下,A单质能置换出C单质
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实能说明氯的非金属性比硫强的是 ( )
A.铁与硫反应生成硫化亚铁,而铁与氯气反应时生成氯化铁
B.与金属钠反应,氯原子得一个电子,而硫原子能得两个电子
C.常温时氯气呈气态,而硫呈现固态
D.氯的最高价为+7价,而硫的最高价为+6价
查看答案和解析>>
科目:高中化学 来源: 题型:
写出下列反应的热化学方程式
(1)在25℃,101 Kpa 下1 mol 乙醇(C2H5OH)完全燃烧并生成二氧化碳和液态水时,放出热量为1366.8 kJ,试写出表示乙醇燃烧的热化学方程式:____
(2)肼(N2H4)又称联氨,是一种可燃性液体,其燃烧热较大且燃烧产物对环境无污染,故可以用作火箭燃料。已知:N2(g)+2O2 (g)=2NO2(g) △H=+67.7kJ/mol
2N2H4(g)+2NO2 (g)=3N2(g)+4H2O(g)△H= 一1135.7kJ/ mol
则肼完全燃烧的热化学方程式为 。
(3)高炉炼铁中发生的基本反应之一如下:
FeO(s)+ CO(g)= Fe(s)+ CO2(g) △H>0。
①此反应的平衡常数表达式为 ;
②温度升高平衡常数K值 (填“增大”、“减小”、或“不变”)
③已知1100℃时,K= 0.263,此时测得高炉中c(CO2)= 0.025mol/L,c(CO)= 0.1mol/L,在这种情况下,该反应 (填“是”或“不是” )处于化学平衡状态,此时化学反应速率是
)处于化学平衡状态,此时化学反应速率是
v正 v逆(填“<”、“>”或“=”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com