
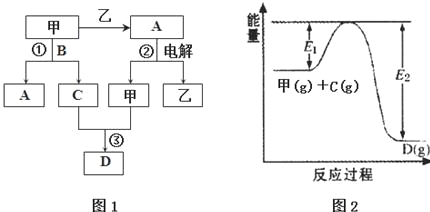
| 容器编号 | n(甲) | n(C) | n (D) | v正与v逆的关系 |
| Ⅰ | 0.20 | 0.10 | 0.20 | v正=v逆 |
| Ⅱ | 0.20 | 0.40 | 1.00 | ②? |
| Ⅲ | 0.60 | 1.20 | 0.80 | ③? |
分析 (1)(2)A、B、C、D都是中学化学中的常见化合物,均由周期表前18号元素组成,D为红综色气体,则D为NO2,甲、乙是两种单质,甲和乙反应生成A,电解A生成甲和乙,且C能和甲反应生成二氧化氮,反应①②均是工业生产中的重要反应,故甲为O2,乙是Al,A是Al2O3,氧气和B反应生成E和C,C和氧气反应生成二氧化氮,所以C是NO,B是NH3;
(3)反应③为:2NO+O2?2NO2 ,根据图2知,该反应是放热反应,提高一氧化氮的转化率,可以采取的措施有:降低温度、增大压强、增大氧气的量、减少二氧化氮的量等;
(4)根据2NO+O2?2NO2 可知,反应后气体物质的量减少的量等于参加反应的氧气的量,再根据v=$\frac{\frac{△n}{V}}{△t}$计算用氧气表示的化学反应速率;
(5)反应(3)中的反应为:2NO+O2?2NO2 ,I处于平衡状态,根据K=$\frac{c{\;}^{2}(NO{\;}_{2})}{c{\;}^{2}(NO)•c(O{\;}_{2})}$计算平衡常数,计算II、Ⅲ中浓度熵Qc,与平衡常数比较判断反应进行方向,进而判断v正、v逆的相对大小.
解答 解:A、B、C、D都是中学化学中的常见化合物,均由周期表前18号元素组成,D为红综色气体,则D为NO2,甲、乙是两种单质,甲和乙反应生成A,电解A生成甲和乙,且C能和甲反应生成二氧化氮,反应①②均是工业生产中的重要反应,故甲为O2,乙是Al,A是Al2O3,氧气和B反应生成E和C,C和氧气反应生成二氧化氮,所以C是NO,B是NH3,
(1)甲和乙发生化合反应,电解A是氧气和水属于分解反应,该反应中没有复分解反应和置换反应,故选:cd;
(2)反应①的化学方程式是:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,故答案为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;
(3)反应③为:2NO+O2?2NO2 ,根据图2知,该反应是放热反应,则反应方程式为:2NO+O2?2NO2 △H<0,提高一氧化氮的转化率,可以采取的措施有:降低温度、增大压强、增大氧气的量、减少二氧化氮的量,而使用催化剂,加快反应速率,不影响平衡移动,加入NO,平衡向正反应方向移动,但NO的转化率降低,故选:BC;
(4)若将1 molO2和2mol NO混合充入容积为2L的密闭容器中,3分钟后反应达到平衡.平衡后混合气体总物质的量为2.55mol,根据2NO+O2?2NO2 可知,反应后气体物质的量减少的量等于参加反应的氧气的量,故参加反应氧气为1mol+2mol-2.55mol=0.45mol,则用氧气表示的化学反应速率=$\frac{\frac{0.45mol}{2L}}{3min}$=0.075 mol/(L•min),
故答案为:0.075;
(5)反应(3)中的反应为:2NO+O2?2NO2 ,I处于平衡状态,故该温度下的平衡常数K=$\frac{c{\;}^{2}(NO{\;}_{2})}{c{\;}^{2}(NO)•c(O{\;}_{2})}$=$\frac{(\frac{0.2}{2})^{2}}{(\frac{0.1}{2})^{2}(\frac{0.2}{2})}$=20,
II中反应的浓度熵Qc=$\frac{0.{5}^{2}}{0.{2}^{2}×0.05}$=125>20,反应向逆反应进行,故v正<v逆,
Ⅲ中反应的浓度熵Qc=$\frac{0.{4}^{2}}{0.{6}^{2}×0.3}$=$\frac{4}{27}$<20,反应向正反应进行,故v正>v逆,
故答案为:20;v正<v逆;v正>v逆.
点评 本题考查无机物推断、化学反应速率计算、化学平衡影响因素、化学平衡常数计算、反应热计算,侧重考查学生对知识迁移运用,需要学生具备知识的基础,难度中等.


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 常温下含有NA个NO2、N2O4分子的混合气体,降温至标准状况,其体积小于22.4 L | |
| B. | 相同条件下,1 L CO和H2的混合气体完全燃烧消耗0.5 L O2 | |
| C. | 标准状况下,44.8 L NO与22.4 L O2充分反应后得到的气体分子数小于2NA | |
| D. | 在常温常压下,2.24 L SO2与O2的混合气体中所含氧原子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeO | B. | Fe2O3 | C. | Fe3O4 | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 白色沉淀是CuI2,棕色溶液含有I2 | |
| B. | 滴加KI溶液时,转移1mol电子时生成1mol白色沉淀 | |
| C. | 通入SO2时,SO2与I2反应,I2作还原剂 | |
| D. | 上述实验条件下,物质的氧化性:I2>Cu2+>SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
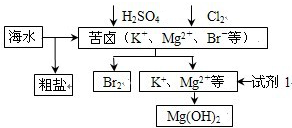
| A. | 试剂1可以选用石灰乳 | |
| B. | 从苦卤中提取Br2的反应的离子方程式为:2Br-+Cl2=2 Cl-+Br2 | |
| C. | 工业上,电解熔融MgO冶炼金属镁可减小能耗 | |
| D. | 粗盐经提纯后可用于制备氯气、钠等产品 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向某溶液中加入氯化钡溶液,有白色沉淀生成,再加盐酸酸化,沉淀不溶解 | 该溶液中一定含有SO42- |
| B | 用洁净的玻璃管向包有Na2O2的脱脂棉吹气,脱脂棉燃烧 | CO2、H2O与Na2O2反应是放热反应 |
| C | 向某溶液中加入稀盐酸,产生能使澄清石灰水变浑浊的无色无味气体 | 该溶液中一定含有CO32- |
| D | 用铂丝蘸取某溶液在无色火焰上灼烧直接观察火焰颜色未见紫色 | 原溶液中不含K+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
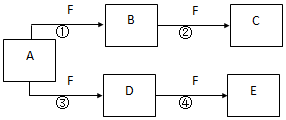 X、Y、Z是三种短周期元素,X和Z的质子数之和与Y的质子数相等,Z的电子层数是X的电子层数的2倍.A、B、C、D、E、F是中学化学中的常见物质,它们由上述三种元素中的一种、两种或三种组成,其中A是能使湿润红色石蕊试纸变蓝的气体,D、E是两种酸,D的钠盐是一种致癌物质,F是一种单质,反应③④均在微生物作用下进行,其转化关系如图所示.回答下列问题:
X、Y、Z是三种短周期元素,X和Z的质子数之和与Y的质子数相等,Z的电子层数是X的电子层数的2倍.A、B、C、D、E、F是中学化学中的常见物质,它们由上述三种元素中的一种、两种或三种组成,其中A是能使湿润红色石蕊试纸变蓝的气体,D、E是两种酸,D的钠盐是一种致癌物质,F是一种单质,反应③④均在微生物作用下进行,其转化关系如图所示.回答下列问题: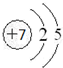 ,A的电子式为
,A的电子式为 ,
,查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com