


 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:
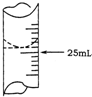 欲测定某NaOH溶液的物质的量浓度,可用物质的量浓度为0.1000mol?L-1 HCl标准溶液进行中和滴定(用酚酞作指示剂).
欲测定某NaOH溶液的物质的量浓度,可用物质的量浓度为0.1000mol?L-1 HCl标准溶液进行中和滴定(用酚酞作指示剂).| 实验序号 | 待测NaOH溶液的体积/mL | HCl标准溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 0.00 | 20.10 |
| 2 | 25.00 | 1.50 | 21.40 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 加入食盐 |
| Ⅰ |
| 通入足量气体B |
| Ⅱ |
| 过滤 |
| Ⅲ |
| Ⅳ |
| A、A气体是NH3,B气体是CO2 |
| B、第Ⅲ步得到的晶体是发酵粉的主要成分 |
| C、第Ⅲ步操作用到的主要玻璃仪器是烧杯、漏斗、玻璃棒 |
| D、第Ⅳ步操作的主要过程有溶解、蒸发、结晶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、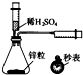 测定一定时间内生成H2的反应速率 |
B、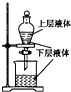 提取海带中的碘 |
C、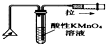 检验火柴燃烧产生的SO2 |
D、 证明非金属性:Cl>C>Si |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用10mL量筒量取7.13mL稀盐酸 |
| B、用酸式滴定管量取13.17mL稀盐酸 |
| C、用广泛pH试纸测得某溶液的pH为2.3 |
| D、用天平称取物品的质量为5.872g |
查看答案和解析>>
科目:高中化学 来源: 题型:
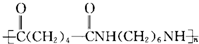 ,
,| A、HOOCCH2CH2CH2CH2CH2CH2COOH和H2NCH2CH2CH2CH2CH2CH2NH2 |
| B、HOOCCH2CH2CH2CH2CH2CH2COOH和H2NCH2CH2CH2CH2NH2 |
| C、HOOCCH2CH2CH2CH2CH2CH2NH2 |
| D、HOOCCH2CH2CH2CH2COOH和H2NCH2CH2CH2CH2CH2CH2NH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
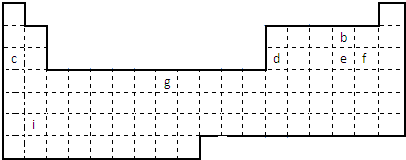
查看答案和解析>>
科目:高中化学 来源: 题型:
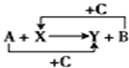 已知A、B、C是单质且C是绿色植物光合作用的产物之一,X、Y是化合物,它们之间的转化关系如图(反应条件略).下列A、B间的对应关系,不正确的是( )
已知A、B、C是单质且C是绿色植物光合作用的产物之一,X、Y是化合物,它们之间的转化关系如图(反应条件略).下列A、B间的对应关系,不正确的是( )| A、A是铝,B是铁 |
| B、A是碳,B是硅 |
| C、A是氢气,B是铜 |
| D、A是钠,B是氢气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com