
【题目】A、B、C、D四种元素,它们原子的核电荷数均小于18,且依次递增,A原子核内仅有一个质子;B原子的电子总数与D原子的最外层电子数相等;A原子与B原子的最外层电子数之和与C原子的最外层电子数相等;D原子有两个电子层,最外层电子数是次外层电子数的3倍。
(1)试推断写出它们的元素符号:A______,B______,C______,D______。
(2)画出D的离子结构示意图___________________。
(3)由这四种元素组成的三核10电子的分子式是_________ ,写出该分子的电子式 _________。
【答案】H C N O ![]() H2O
H2O ![]()
【解析】
A、B、C、D四种元素,它们原子的核电荷数均小于18,且依次递增.A原子核内仅有1个质子,则A为氢元素;D原子的最外层电子数是次外层电子数的3倍,最外层电子数不超过8,原子只能有2个电子层,最外层电子数为6,故D为O元素;B原子的电子总数与D原子的最外层电子数相等,则B为C元素;A原子与B原子的最外层电子数之和与C原子的最外层电子数相等,则C原子最外层电子数为1+4=5,其原子序数小于氧,故C为N元素,据此进行解答。
A、B、C、D四种元素,它们原子的核电荷数均小于18,且依次递增.A原子核内仅有1个质子,则A为氢元素;D原子的最外层电子数是次外层电子数的3倍,最外层电子数不超过8,原子只能有2个电子层,最外层电子数为6,故D为O元素;B原子的电子总数与D原子的最外层电子数相等,则B为C元素;A原子与B原子的最外层电子数之和与C原子的最外层电子数相等,则C原子最外层电子数为1+4=5,其原子序数小于氧,故C为N元素,
(1)根据分析可知,A为H、B为C、C为N、D为O元素,故答案为:H;C;N;O;
(2)D为O元素,原子序数为8,氧离子的核外电子总数为10,其离子结构示意图为: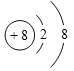 ,故答案为:
,故答案为: ;
;
(3)A为H、B为C、 C为N、D为O元素,由这四种元素组成的三核10电子的化合物为水,其分子式为:H2O;电子式为:![]() ,故答案为:H2O;
,故答案为:H2O;![]() 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】南海是一个巨大的资源宝库,开发利用这些资源是科学研究的重要课题。下图为海水资源利用的部分过程,有关说法正确的是( )
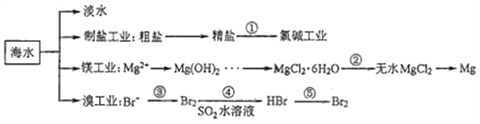
A. 海水淡化的方法主要有蒸馏法、电渗析法、冰冻法
B. 氯碱工业中采用阴离子交换膜可提高产品的纯度
C. 由MgCl2·6H2O得到无水MgCl2的关键是要低温小火烘干
D. 溴工业中③、④的目的是为了富集溴元素,溴元素在反应③、⑤中均被氧化,在反应④中被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应速率和限度与生产、生活密切相关。
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如表(累计值):
时间(min) | 1 | 2 | 3 | 4 | 5 |
氢气体积(mL)(标准状况) | 100 | 240 | 464 | 576 | 620 |
①哪一时间段反应速率最大___min(填0~1、1~2、2~3、3~4、4~5)。反应开始后反应速率先增大的原因是__。
②求3~4分钟时间段以盐酸的浓度变化来表示的该反应速率__________(设溶液体积不变)。
(2)另一学生为控制反应速率防止反应过快难以测量氢气体积,他事先在盐酸中加入少量的下列溶液以减慢反应速率,你认为不可行的是_。
A.蒸馏水 B.KCl溶液 C.KNO3溶液 D.CuSO4溶液
(3)某温度下在4L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图
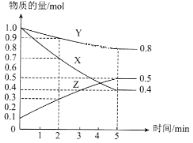
①该反应的化学方程式是__________。
②该反应达到平衡状态的标志是__________。
A.X、Y、Z的反应速率相等 B.容器内气体密度保持不变 C.容器内气体压强保持不变 D.消耗3molX的同时生成1mol Y
③2min内X的转化率为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌在工业中有重要作用,也是人体必需的微量元素。回答下列问题:
(1)Zn原子核外电子排布式为________________。
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能Ⅰ1(Zn)_____Ⅰ1(Cu)(填“大于”或“小于”)。原因是_____________________________。
(3)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为________________,C原子的杂化形式为________________,SO42-、CS2、CO32-键角由大到小的顺序是______________________
(4)锌冶炼过程中会产生污染性气体二氧化硫,已知液态二氧化硫也可以发生类似水的自身电离2SO2![]() SO2++SO32-,S和O两种元素中电负性较强的是______________,与SO2+互为等电子体的单质分子是________(填化学式),SO2+中σ键和兀键数目比为___________。
SO2++SO32-,S和O两种元素中电负性较强的是______________,与SO2+互为等电子体的单质分子是________(填化学式),SO2+中σ键和兀键数目比为___________。
(5)分析并比较物质A: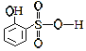 与B:
与B: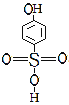 的沸点高低及其原因:__
的沸点高低及其原因:__
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在常用催化剂(如铂、钯)的催化下,氢气和炔烃加成生成烷烃,难于得到烯烃,但使用活性较低的林德拉催化剂,可使炔烃的氢化停留在生成烯烃的阶段,而不再进一步氢化.现有一课外活动兴趣小组利用上述设计了一套由如下图所示仪器组装而成的实验装置(铁架台未画出),拟由乙炔制得乙烯,并测定乙炔氢化的转化率.若用含0.020molCaC2的电石和1.60g含杂质18.7%的锌粒(杂质不与酸反应)分别与足量的X和稀硫酸反应,当反应完全后,假定在标准状况下测得G中收集到的水VmL.试回答有关问题.
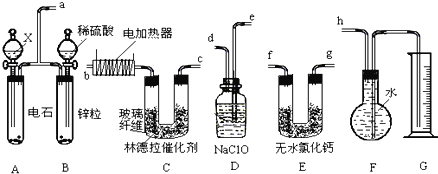
(1)所用装置的连接顺序是_______________(填各接口的字母).
(2)写出A、C中所发生的两个反应的化学方程式(有机物写结构简式):__________、_____________.
(3)为减慢A中的反应速率,X应选用_________.
(4)F中留下的气体除含少许空气外,还有________________.
(5)D的作用是_________________
(6)若V=672mL(导管内气体体积忽略不计),则乙炔氢化的转化率为_____________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A.钠和冷水反应:Na+2H2O=Na++2OH-+H2↑
B.金属铝溶于氢氧化钠溶液:Al+2OH-=![]() +H2↑
+H2↑
C.金属铝溶于盐酸中:2Al+6H+=2Al3++3H2↑
D.碳酸氢钠溶液中滴入少量的氢氧化钙溶液:HCO3-+OH-= CO32-+ H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将下列物质进行分类(填序号)
①O2与O3 ②![]() C与
C与![]() C ③H2O和D2O ④冰与干冰 ⑤H2、D2、T2 ⑥乙醇与乙醚(CH3-O-CH3) ⑦CH3CH2CH2CH2CH3和CH3CH2CH2CH2CH3
C ③H2O和D2O ④冰与干冰 ⑤H2、D2、T2 ⑥乙醇与乙醚(CH3-O-CH3) ⑦CH3CH2CH2CH2CH3和CH3CH2CH2CH2CH3
(1)互为同位素的是___;
(2)互为同素异形体的是___;
(3)互为同分异构体的是___;
(4)属于同一化合物的是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化锰在工业上具有重要的作用,工业上可利用菱锰矿(主要成分为MnCO3、SiO2、FeCO3以及少量CuO)制取。制备流程如图所示:
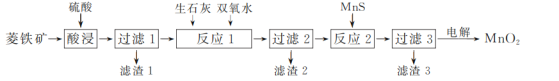
(1)酸浸过程中,MnCO3溶解的离子方程式为______,选择用硫酸而不选择盐酸溶解,除了盐酸挥发造成设备腐蚀以外,另一个原因是________。
(2)滤渣3的主要成分是________,除铁的过程中,应该先加________(填“生石灰”或“双氧水”),原因是__________。
(3)用惰性电极对过滤3得到的滤液进行电解,得到MnO2,写出电解过程中阳极电极反应式:__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com