
某温度下,将Cl2通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合液,经测定NaClO与NaClO3的浓度之比为l:3 , 则C12与NaOH溶液反应时被还原的氯元素与被氧化的氯元素的物质的量之比为( )
A.21:5 B.11:3 C.3:1 D.4:1
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源:2017届江苏省高三上学期摸底考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.若1mol Na2O2与足量水反应后产生氧气,理论上转移的电子数为2×6.02×1023
B.0.1mol/L Na2CO3溶液加热后,溶液的pH减小
C.室温下稀释0.1mol/L CH3COOH溶液,溶液的导电能力减弱,因此溶液中所有离子浓度均减小
D.向废水中滴加FeCl3饱和溶液制备Fe(OH)3胶体的原理是加热促进Fe3+水解
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省汕头市高二上学期入学考试化学试卷(解析版) 题型:推断题
某混合溶液中可能含有HCl、MgCl2、AlCl3、NH4Cl、Na2CO3、KCl中的几种物质,往该溶液中逐滴加入NaOH溶液,产生沉淀的物质的量(n)与加入的NaOH溶液体积(V)的关系如图所示。回答下列问题:
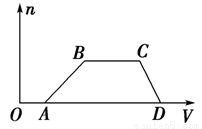
(1)溶液中一定含有的溶质是______________(填化学式)。
(2)溶液中一定不含有的溶质是____________(填化学式)。
(3)溶液中可能含有的溶质是__________(填名称),判断该物质是否存在的实验方法是________,现象是_____________。
(4)分别写出AB段、BC段发生的离子方程式:
①AB段为________________________________;
②BC段为________________________________。
查看答案和解析>>
科目:高中化学 来源:2017届新疆生产建设兵团二中高三上第一次月考化学试卷(解析版) 题型:填空题
铈、铬、钛、镍虽不是中学阶段常见的金属元素,但在工业生产中有着重要作用。
(1)二氧化铈 (CeO2)在平板电视显示屏中有着重要应用.CeO2在稀硫酸和H2O2的作用下可生成Ce3+,写出该反应的化学方程式__________________,CeO2在该反应中作__________剂。
(2)自然界中Cr主要以+3价和+6价存在.+6价的Cr能引起细胞的突变,可以用亚硫酸钠将其还原为+3价的铬.写出过程中的离子方程式:________________。
(3)钛(Ti)被誉为“二十一世纪的金属”,工业上在550℃时用钠与四氯化钛反应可制得钛,该反应的化学方程式是_________________。
(4)NiSO4·xH2O是一种绿色易溶于水的晶体,广泛用于镀镍、电池等,可由电镀废渣(除镍外,还含有铜、锌、铁等元素)为原料获得.操作步骤如下:
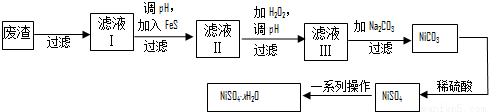
①向滤液Ⅰ中加入FeS是为了除去Cu2+、Zn2+等杂质,除去Cu2+的离子方程式为__________。
②对滤液Ⅱ先加H2O2再调pH,加H2O2的目的是_____________,调pH的目的是____________。
③滤液Ⅲ溶质的主要成分是NiSO4,加Na2CO3过滤后,再加适量稀硫酸溶解又生成NiSO4,这两步操作的目的是__________________。
查看答案和解析>>
科目:高中化学 来源:2017届新疆生产建设兵团二中高三上第一次月考化学试卷(解析版) 题型:选择题
分子式为C5H12O的有机物含有-CH2OH基团同分异构体有( )
A.2种 B.3种 C.4种 D.5种
查看答案和解析>>
科目:高中化学 来源:2017届新疆生产建设兵团二中高三上第一次月考化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是( )
A.铜片放入稀硫酸中:Cu+2H+=Cu2++H2↑
B.将少量NaOH溶液加入NH4HCO3溶液中:OH-+HCO3-=CO32-+H2O
C.向NaHCO3溶液中加入少量Ca(OH)2: HCO3-+Ca2++OH-=CaCO3↓+H2O
D.Fe3O4与稀HNO3反应:Fe3O4+8H+=Fe2++2Fe3++4H2O
查看答案和解析>>
科目:高中化学 来源:2017届新疆生产建设兵团二中高三上第一次月考化学试卷(解析版) 题型:选择题
下列金属中,表面自然形成的氧化层能保护内层金属不被空气氧化的是( )
A.K B.Na C.Fe D.Al
查看答案和解析>>
科目:高中化学 来源:2017届河南省高三上第一次周练化学试卷(解析版) 题型:填空题
硫单质及其化合物在工农业生产中有着重要的应用。
(1)已知25℃时:SO2(g)+2CO(g)=2CO2(g)+1/x Sx(s) △H=akJ/mol
2COS(g)+SO2(g)=2CO2(g)+3/x Sx(s) △H=bkJ/mol。
则COS(g)生成CO(g)与Sx(s)反应的热化学方程式是 。
(2)雌黄(As2S3)是提取砷的主要矿物原料。已知As2S3可以和浓HNO3反应,当生成0.6mol的H3AsO4时,反应中转移电子的数目为3NA,则As2S3和浓HNO3反应的方程式是
(3)向等物质的量浓度Na2S、NaOH混合溶液中滴加稀盐酸至过量。其中H2S、HS?、S2?的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与滴加盐酸体积的关系如下图所示(忽略滴加过程H2S气体的逸出)。
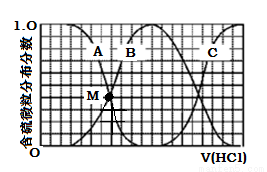
①曲线B表示 的分布分数。
②滴加过程中,溶液中微粒浓度大小关系正确的是 (填字母)。
A.c(Na+)= c(HS?)+2c(S2?)
B.3c(H2S)+2c(HS?)+c(S2?)+c(H+)=c(OH?)
C.3c(Na+)=[c(H2S)+c(HS?)+c(S2?)]
③NaHS溶液呈碱性,当滴加盐酸至M点(A、B曲线的交叉点)时,溶液中各离子浓度由大到小的顺序为
(4)工业上用硫碘开路循环联产氢气和硫酸的工艺流程如下图所示:
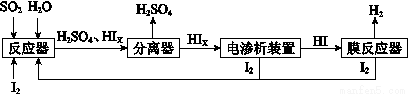
①写出反应器中发生反应的化学方程式是 。
②电渗析装置如下图所示
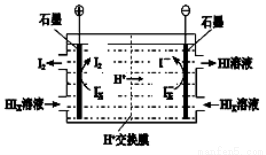
写出阳极的电极反应式 。
该装置中发生的总反应的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省葫芦岛市六校协作体高二上期初考试化学卷(解析版) 题型:选择题
下列反应的离子方程式书写正确的是( )
A.硅酸钠溶液与醋酸溶液混合:SiO32-+2H+=H2SiO3↓
B.NaHCO3溶液中加入过量的 Ba(OH)2溶液:HCO3-+Ba2++OH-= BaCO3↓+H2O
C.氯化铝溶液中加入过量氨水 Al3++ 4NH3·H2O=AlO2-+ 4NH4++2H2O
D.用稀HNO3溶解FeS固体:FeS+2H+=Fe2++H2S↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com