

| A. | A酸比B酸的电离程度小 | |
| B. | A是强酸,B是弱酸 | |
| C. | pH=1时,B酸的物质的量浓度比A酸大 | |
| D. | 将pH=1的A酸和B酸稀释成pH=5的溶液,A酸所需加入的水量多 |
分析 常温下pH=1的两种一元酸溶液A和B,分别加水稀释至1000倍,图象中A的溶液PH变化大,B溶液PH变化小,说明A溶液的酸性大于B溶液酸性,
解答 解:A.上述分析可知A酸比B酸的电离程度大,故A错误;
B.图象变化只能说明A的酸性强于B,只有a=4才能说明A为强酸,故B错误;
C.上述分析可知A酸比B酸的电离程度大,pH=1时,B酸的物质的量浓度比A酸大,故C正确;
D.将pH=1的A酸和B酸稀释成pH=5的溶液,A酸比B酸的电离程度大,B酸溶液浓度大,所以B酸所需加入的水量多,故D错误;
故选C.
点评 本题考查了弱电解质溶液稀释溶液PH变化,图象的理解应用,掌握基础是解题关键,题目难度中等.


 特高级教师点拨系列答案
特高级教师点拨系列答案科目:高中化学 来源: 题型:选择题
| A. | 同一主族元素原子序数越大的单质的熔点、沸点也越高 | |
| B. | 除H外,周期表中主族族序数等于周期数的元素全为金属元素 | |
| C. | 同主族的非金属的简单氢化物中最稳定的其熔、沸点也最高 | |
| D. | 同周期的主族元素形成的简单离子的半径从左到右依次减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数:b>a>c>d | B. | 原子半径:C>D>A>B | ||
| C. | 离子半径:Cn->D(n+1)->An+>B(n+1)+ | D. | 单质还原性:A>B>C>D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 弱酸化学式 | HClO | H2CO3 |
| 电离平衡常数 | K=4.7×10-8 | K1=4.3×10-7,K2=5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
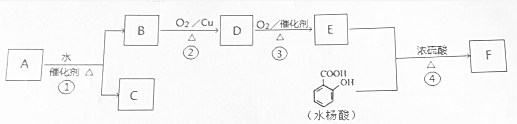
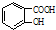 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$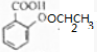 +H2O.
+H2O. $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$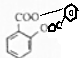 +H2O.
+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝表面易形成一层致密的氧化膜保护层,故铝可以广泛用于制造炊具和包装食品 | |
| B. | 5.6gFe在纯氧中燃烧和与足量水蒸气反应,转移电子的物质的量均为$\frac{0.8}{3}$mol | |
| C. | 金属钠在空气中燃烧得到白色固体 | |
| D. | 钠着火时,可直接用水灭火 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
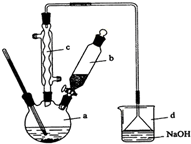 溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如表:
溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如表:| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇和乙二醇属于同系物 | |
| B. | 1-丁烯存在顺反异构体 | |
| C. | 将苯加入溴水中,溴水褪色,是因为发生了加成反应 | |
| D. | 分子式为C3H8与C6H14的两种有机物一定互为同系物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com