
| A. | LiNiO2中Ni的化合价是+1 | |
| B. | 该反应中LiOH是还原剂 | |
| C. | OH-和Li+含有的电子数相同 | |
| D. | 该反应生产1mol LiNO2时转移1 mole- |
分析 A、依据锂元素为+1价,氧元素为-2价可知Ni元素化合价为+3价;
B、依据化学方程式中元素化合价变化分析,锂元素化合价不变;
C、氢氧根离子含有10个电子,锂离子含有2个电子;
D、4Ni(OH)2+4LiOH+O2═4LiNiO2+5H2O反应中生成4mol LiNO2时转移4mole-.
解答 解:A、LiNi02中锂元素为+1价,氧元素为-2价可知Ni元素化合价为+3价,故A错误;
B、4Ni(OH)2+4LiOH+O2=4LiNiO2+6H2O,反应前后锂元素化合价不变,不是还原剂,故B错误;
C、氢氧根离子含有10个电子,锂离子含有2个电子,电子数不同,故C错误;
D、由4Ni(OH)2+4LiOH+O2═4LiNiO2+5H2O反应中生成4mol LiNO2时转移4mole-,所以生产1mol LiNO2时转移1 mole-,故D正确;
故选D.
点评 本题考查了氧化还原反应的元素化合价变化,离子结构的分析判断,题目难度中等.


 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:选择题
| A. | CH4 C2H4 | B. | CH4 C3H6 | C. | C2H4 C3H4 | D. | C2H4 CH4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
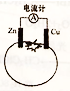
| A. | 一段时间后,锌片质量会减少 | B. | 一段时间后,铜片质量会减少 | ||
| C. | 电流由铜通过导线流向锌 | D. | 锌电极是该电池的负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 强酸性溶液中:Mg2+、K+、SO42-、NO3- | |
| B. | 强碱性溶液中:Na+、Cu2+、H CO3-、NO3- | |
| C. | AgNO3 溶液中:H+、K+、SO42-、Cl- | |
| D. | Ba(NO3)2 溶液中:Mg2+、K+、SO42-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
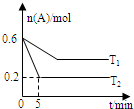 一定条件下,反应A(g)?B(g)+C(g) 在2.0L的密闭容器中进行,在T1和T2两个温度下A的物质的量与时间的关系如图所示.下列有关说法正确的是( )
一定条件下,反应A(g)?B(g)+C(g) 在2.0L的密闭容器中进行,在T1和T2两个温度下A的物质的量与时间的关系如图所示.下列有关说法正确的是( )| A. | 正反应△H>0 | |
| B. | 平衡常数K(T2)<K(T1) | |
| C. | T2时,达到平衡时A的转化率为33.3% | |
| D. | T2时,该反应的化学平衡常数为0.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它们都是金属元素 | B. | 它们的原子半径相差不大 | ||
| C. | 它们的最外层电子数相同 | D. | 它们的最高化合价相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
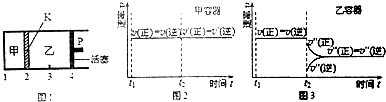
| A. | 保持活塞位置不变,升高温度,达到新的平衡后,甲、乙中B的体积分数分别为增大和减小 | |
| B. | 保持温度和活塞位置不变,在甲中再加入1mol A和2mol B,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍 | |
| C. | 保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率 变化已省略) | |
| D. | 保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com