
【题目】下图是工业上铝土矿(含有Al2O3和Fe2O3等)冶炼铝的工艺流程图:
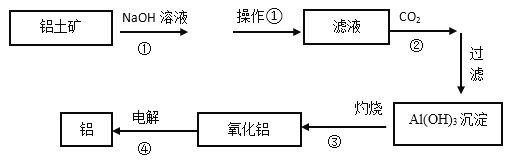
(1)操作①的名称是:_________。操作①剩余的矿渣主要成分为:__________(填化学式)。
(2)图中①的离子方程式___________________________;④的化学反应方程式___________。
(3)洗涤Al(OH)3沉淀的具体操作是: ________________________________________。
【答案】过滤 Fe2O3 Al2O3+2OH-=2AlO2-+H2O 2Al2O3(熔融)![]() 4Al+3O2↑ 往漏斗中加水至浸没沉淀,待水自然流下,重复操作2-3次
4Al+3O2↑ 往漏斗中加水至浸没沉淀,待水自然流下,重复操作2-3次
【解析】
Al2O3、Fe2O3都和硫酸反应,要将氧化铝和Fe2O3分离出来,应该选择氢氧化钠,将氧化铝溶解为偏铝酸钠,剩余固体难溶物氧化铁,操作①是过滤,沉淀中含有氧化铁,滤液是偏铝酸钠溶液,偏铝酸钠中通二氧化碳来获得氢氧化铝沉淀,发生CO2+AlO2-+2H2O=Al(OH)3↓+HCO3-,过滤,氢氧化铝沉淀加热分解生成氧化铝,电解可得铝,以此解答该题。
(1)根据以上分析操作①是用来分离Fe2O3和偏铝酸钠溶液,固液分离应该选择过滤,操作①剩余的矿渣主要成分为Fe2O3;
答案:过滤 Fe2O3
(2)图中①Al2O3与氢氧化钠反应的离子方程式Al2O3+2OH-=2AlO2-+H2O;反应④电解熔融的氧化铝用来冶炼铝,化学反应方程式2Al2O3(熔融)![]() 4Al+3O2↑;
4Al+3O2↑;
答案:Al2O3+2OH-=2AlO2-+H2O 2Al2O3(熔融)![]() 4Al+3O2↑
4Al+3O2↑
(3)洗涤沉淀通常采用淋洗法,即往漏斗中加水至浸没沉淀,待水自然流下,重复操作2-3次;
答案:往漏斗中加水至浸没沉淀,待水自然流下,重复操作2-3次


 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源: 题型:
【题目】关于0.1mol·L-1 Na2CO3溶液的叙述错误的是( )
A.0.5 L该溶液中,Na+的物质的量浓度为0.2mol·L-1
B.1 L该溶液中,含CO32—的数目小于0.1NA(NA是阿伏加德罗常数)
C.从1 L该溶液中取出100 mL,则取出的溶液中Na2CO3的物质的量浓度为0.01mol·L-1
D.取该溶液10 mL,加水稀释至100 mL后,Na2CO3的物质的量浓度为0.01mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知: A是石油裂解气的主要成份且A的产量通常用来衡量一个国家的石油化工水平;D是常用作厨房中调味品。请回答下列问题:
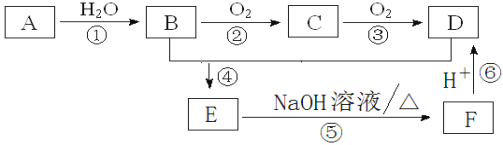
(1)写出C的结构简式________________________。
(2)写出下列反应的反应类型: ①________________,④________________。
(3)写出下列反应的化学方程式:
②______________________________________________________________。
⑤______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列填空
(1)检验铁离子(Fe3+):试剂____________(填化学式);现象______________。有铁离子(Fe3+)的环境下检验是否含有亚铁离子(Fe2+):试剂:_________(填化学式),现象_______________。
(2)用小苏打片治疗胃酸过多的离子方程式为____________。
(3)镁带着火时,不能用液态CO2灭火剂来灭火的原因是_____________。(用化学方程式表示).
(4)除去混入Fe2O3粉末中少量Al2O3杂质离子方程式为______________。
(5)将AlCl3溶液蒸干,灼烧,得到的固体产物是__________。AlCl3溶液和NaHCO3溶液混合时发生反应的离子方程式为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有X、Y、Z、W、Q五种短周期元素在周期表中的相对位置如下所示,其中Z原子的核外电子数是其价电子数的3倍,Q的一种核素没有中子。
X | Y | |
Z | W |
请回答下列问题:
(1)元素W在元素周期表中的位置是___________________________;
(2)画出Z的原子结构示意图______________;QXY的电子式为_________________;
(3)Y的最高价氧化物的化学式为_________;
(4)W和Y形成的一种二元化合物具有色温效应,其相对分子质量在170~190之间,且W的质量分数约为70%。该化合物的化学式为_________________;
(5) (XY)2称为拟卤素,性质与卤素类似,其与氢氧化钠溶液反应的化学方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某市的“二期课改”中,初中化学引入“物质的量”的教学内容。物质的量是一种新的物理量,其单位是摩尔(mol),1摩尔物质大约含有6.02×1023个该物质的微粒.如1mol氢气含有6.02×1023个H2分子,含有2×6.02×1023个H原子。据此回答:
(1)物质的量与物质的质量、物质的数量是___(填“相同”或“不同”)的物理量。
(2)1mol硝酸中含有___个H原子,含有___个N原子。
(3)如图是氧原子的结构示意图,那么,1mol氧气分子中含有___个电子。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一容积固定的容器中,反应aA(g)+bB(g)![]() hH(g)达到平衡后,A、B、H的物质的量分别为amol、bmol和hmol。已知a+b=2h,若保持温度不变,将三者的物质的量增大一倍,则下列判断正确的是
hH(g)达到平衡后,A、B、H的物质的量分别为amol、bmol和hmol。已知a+b=2h,若保持温度不变,将三者的物质的量增大一倍,则下列判断正确的是
A.平衡不移动B.混合气体的密度不变
C.B的体积分数减少D.amol/L<c(A)<2amol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:CH3—CH![]() CH2 + HBr
CH2 + HBr![]() CH3—CHBr—CH3(主要产物)。1 mol某烃A充分燃烧后得到8molCO2和4molH2O。烃A在不同条件下能发生如下图所示的一系列变化。
CH3—CHBr—CH3(主要产物)。1 mol某烃A充分燃烧后得到8molCO2和4molH2O。烃A在不同条件下能发生如下图所示的一系列变化。
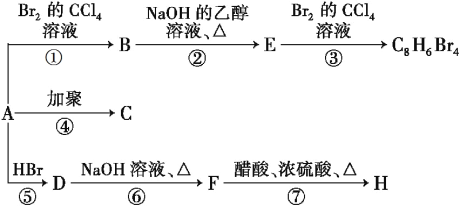
(1)A的结构简式:_______。
(2)上述反应②是_______反应,⑦是_______反应。(填反应类型)
(3)写出C、H物质的结构简式:C_________,H_________。
(4)写出D![]() F反应的化学方程式_______________。
F反应的化学方程式_______________。
(5)化合物G是F的同分异构体,遇FeCl3溶液显紫色,且苯环上只有两种不同化学环境的氢原子,写出符合条件的G的结构简式__________。(任写一种即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一恒温、恒容的密闭容器中发生反应A(s)+2B(g)![]() C(g)+D(g),当下列物理量不再变化时,不能够表明该反应已达平衡状态的是
C(g)+D(g),当下列物理量不再变化时,不能够表明该反应已达平衡状态的是
A.混合气体的压强B.混合气体的平均相对分子质量
C.A的物质的量D.B的物质的量浓度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com