
将1.00 mol·L-1 NaOH溶液滴入20.00 mL 1.00 mol·L-1的一元酸HA溶液中,测得混合溶液的pH和温度随加入NaOH溶液体积变化曲线如图所示。
(1)计算室温时20.00 mL 1.00 mol·L-1的一元酸
HA的电离度α=________。
 (2)图中B点所示的溶液中所含各离子浓度由
(2)图中B点所示的溶液中所含各离子浓度由
大到小的顺序是_____。
(3)下列说法正确的是________(填相应序号)。
A.由图中可知NaOH和HA反应的ΔH>0
B.图中C点所加NaOH溶液的体积V=20.00 mL
C.图中C点时溶液的KW略大于1×10-14 mol·L-1,溶液中c(H+)=1×10-7 mol·L-1
D.图中D点后,溶液温度略下降的主要原因是生成的NaA水解吸热
(4)常温下在20 mL 0.1 mol·L-1 Na2CO3溶液中逐滴加入
0.1 mol·L-1 HCl溶液40 mL,溶液中含碳元素的各种微粒
(CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的
部分情况如图所示。]回答下列问题:
① 在同一溶液中,H2CO3、HCO 、CO
、CO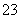
______(填“能”或“不能”)大量共存;
② 当pH=7时,溶液中含碳元素的主要微粒为________,溶液中各种离子的物质的量
浓度的大小关系为________________________________;
③ 已知在25 ℃时,CO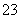 水解反应的平衡常数即水解常数Kh=2×10-4 mol·L-1,当溶
水解反应的平衡常数即水解常数Kh=2×10-4 mol·L-1,当溶
液中c(HCO )∶c(CO
)∶c(CO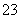 )=2∶1时,溶液的pH=________。
)=2∶1时,溶液的pH=________。
 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源: 题型:
在实验室里,某同学取一小块金属钠做钠与水反应的实验。试完成下列问题:
(1)切开的金属钠暴露在空气中,最先观察到的现象是____________________________,所发生反应的化学方程式是_______________________________________________。
(2)将钠投入水中后,钠熔化成一个小球,根据这一现象你能得出的结论是
①_______________________________________________,
②_______________________________________________。
将一小块钠投入盛有饱和石灰水的烧杯中,不可能观察到的现象是________。
A.有气体生成
B.钠熔化成小球并在液面上游动
C.烧杯底部有银白色的金属钙生成
D.溶液变浑浊
(3)钠与硫酸铜溶液反应的离子方程式为____________________________________。在反应过程中,若生成标准状况下224 mL的H2,则转移的电子的物质的量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中能说明金属A肯定比金属B的活泼性强的是 ( )
A.A原子的最外层电子数比B原子的最外层电子数少
B.A原子电子层数比B原子电子层数多
C.1mol A从酸中置换出的H2比1molB从酸中置换的H2多
D.常温时,A能从稀盐酸中置换出氢,而B不能
查看答案和解析>>
科目:高中化学 来源: 题型:
右下图是周期表中短周期的一部分,A、B、C三种元素的原子核外电子数之和等于B的质量数的2.5倍,B元素的原子核内质子数等于中子数,下列叙述不正确的是( )
| B | ||
| A | C |
A. A为ⅤA族元素 B. B为第二周期的元素
C. C是周期表中化学性质最活泼的非金属
D. 三种元素都为非金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D四种短周期元素原子序数依次增大,A原子为半径最小的原子,C原子最外层电子数与A、 B原子最外层电子数之和相等,D原子和B原子最外层电子数的和为C原子最外层电子数的2倍,D原子的最外层电子数为电子层数的3倍。下列说法正确的是
A.原子半径大小顺序为:B > C > D > A
B.四种元素都属于非金属元素,它们之间只能形成共价化合物
C.B、C元素位于元素周期表中第二周期,D元素位于元素周期表中第三周期
D.BA4、CA 两种微粒都具有正四面体结构,B、C、D三种元素都有属于分子晶体、原子晶体的同素异形体
两种微粒都具有正四面体结构,B、C、D三种元素都有属于分子晶体、原子晶体的同素异形体
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关叙述正确的是
A.非金属氧化物一定为酸性氧化物
B.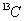 和
和 互为同位素,化学性质相似
互为同位素,化学性质相似
C.根据是否能产生丁达尔效应,将分散系分为溶液、浊液和胶体
D.已知红磷比白磷稳定,则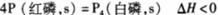
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com