
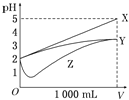
【题目】pH=2的X、Y、Z三种酸的溶液各1mL,分别加水稀释到1000mL,其pH与溶液体积(V)的变化关系如图所示,下列说法中正确的是
A.X是强酸,Y和Z是弱酸
B.稀释前的浓度大小为c(Y)>c(Z)>c(X)
C.稀释前电离程度大小为X>Z>Y
D.pH=2时,X、Y、Z都是稀溶液
【答案】A
【解析】
加水稀释促进弱电解质电离,pH=2的三种酸,稀释1000倍后,如果该酸是强酸,则稀释后溶液pH=5,如果是弱酸,稀释后溶液的pH<5,根据图象知,X是强酸、Y和Z属于弱酸;
加水稀释弱酸过程中,如果弱酸电离增大程度大于溶液体积增大程度,则溶液中氢离子浓度增大,溶液的pH减小,反之,溶液pH增大。
A.加水稀释促进弱电解质电离,pH=2的三种酸,稀释1000倍后,如果该酸是强酸,则稀释后溶液pH=5,如果是弱酸,稀释后溶液的pH<5,根据图象知,稀释1000倍,X溶液的pH=5、Y和Z溶液pH小于5,所以X是强酸、Y和Z属于弱酸,故A正确;
B.pH相等时,弱酸浓度大于强酸,所以Y和Z浓度大于X,根据图象知,刚开始稀释时,Z的pH减小、Y的pH增大,说明Z是浓溶液、Y是稀溶液,则三种酸浓度大小顺序是c(Z)>c(Y)>c(X),故B错误;
C.强电解质X完全电离,Y和Z部分电离,溶液浓度越大其电离程度越小,所以稀释前电离程度大小为X>Y>Z,故C错误;
D.根据B知,pH=2时,X和Y属于稀溶液,Z属于浓溶液,故D错误;
故选:A。


 全程金卷系列答案
全程金卷系列答案 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:
【题目】甲醛(HCHO)俗称蚁醛,是一种重要的有机原料。
I.利用甲醇(CH3OH)制备甲醛
脱氢法:CH3OH(g)=HCHO(g)+H2(g) △H1 = +92.09kJ/mol
氧化法:CH3OH(g) +1/2O2(g)=HCHO(g)+H2O(g) △H2
(1)已知:2H2(g)+O2(g)=2H2O(g) △H3=-483.64 kJ/mol,则△H2=_______。
(2)与脱氢法相比,氧化法在热力学上趋势较大,其原因为_______________。
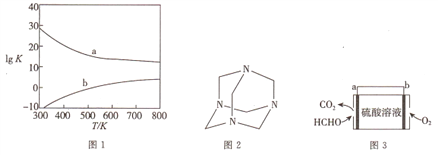
(3)图1为甲醇制备甲醛反应的lg K(K为平衡常数)随温度(T)的变化曲线。曲线____(填“a”或“b”)对应脱氢法,判断依据为_________________。
II.甲醛的用途
(4)将甲醛水溶液与氨水混合蒸发可制得乌洛托品(结构简式如图2),该物质在医药等工业中有广泛用途。若原料完全反应生成乌洛托品,则甲醛与氨的物质的量之比为_______。
(5)将甲醛水溶液与硫酸镍(NiSO4)混合,可用于化学镀镍。若反应过程中有CO2产生,则该反应的离子方程式为____________________。
Ⅲ.甲醛的检测
(6)室内甲醛超标会危害人体健康,通过传感器可以监测空气中甲醛的含量。一种燃料电池型甲醛气体传感器的原理如图3所示,则b极的电极反应式为_________,当电路中转移4×10-4 mol电子时,传感器内参加反应的HCHO为_______mg。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列说法正确的是
A.13 g13 C含有的中子数目为6 NA
B.常温下 ,I LpH =4的醋酸溶液所含离子总数为2 ×10-4NA
C.100 g质量分数为 98% 的磷酸中所含氧原子总数为4 NA
D.0.1 mol Fe 完全溶于稀硝酸,转移的电子数目为0.3 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近科学家研制的一种新型“微生物电池”可以将污水中的有机物转化为H2O和CO2,同时产生电能,其原理示意如图。下列有关该电池的说法正确的是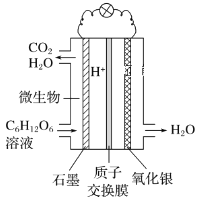
A.氧化银电极上的反应为Ag2O+2e-=2Ag+O2-
B.石墨电极上的反应为C6H12O6+6H2O-24e-=6CO2↑+24H+
C.每转移4 mol电子,石墨电极产生22.4 L CO2气体
D.每30 g C6H12O6参与反应,有4 mol H+经质子交换膜进入负极区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关.
(1)下列生活用品中,其主要材料属于天然纤维的是_________(填字母序号);
A.塑料保鲜薄 B.橡胶手套 C.棉布围裙
(2)我们常用的洗涤剂清洗餐具上的油污,这是因为洗涤剂具有_________的功能;
(3)食用水果、蔬菜主要补充人体所需的_________;
(4)国家禁止在面粉中添加增白剂过氧化钙CaO2,过氧化钙中氧元素的化合价为_______;
(5)农业上降低土壤酸性的是_________(填化学式);
(6)生活中要用到大量的钢铁,写出赤铁矿(主要成分Fe2O3)冶炼成铁的化学方程式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2020年2月,国家卫生健康委办公厅、国家中医药管理局办公室联合发出《关于印发新型冠状病毒肺炎诊疗方案(试行第六版)的通知》。此次诊疗方案抗病毒治疗中增加了磷酸氯喹和阿比多尔两个药物。其中阿比多尔中间体I的合成路线如下:
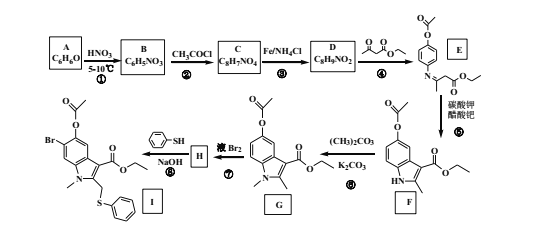
(1)A的结构简式是 _____。描述检验 A的方法及现象______________。
(2)I中含氧官能团名称是_____。
(3)③、⑦的反应类型分别是 ____ 、 __________ 。
(4)②的化学方程式为 ____。
(5)D的同分异构体中,满足下列条件的有_______种
a. 含有苯环 b.含有—NO2
其中核磁共振氢谱为3组峰,且峰面积之比为1∶2∶6的为__________________(任写一种结构简式)。
(6)已知:①当苯环有RCOO-、烃基时,新导入的基团进入原有基团的邻位或对位;原有基团为—COOH时,新导入的基团进入原有基团的邻位。②苯酚、苯胺(![]() )易氧化。设计以
)易氧化。设计以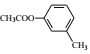 为原料制备
为原料制备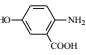 的合成路线 __________(无机试剂任用)。
的合成路线 __________(无机试剂任用)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,向2L密闭容器中加入2molN2和10molH2,发生反应N2(g)+3H2(g)![]() 2NH3(g),2min时测得剩余N2为1mol,下列化学反应速率表示不正确的是( )
2NH3(g),2min时测得剩余N2为1mol,下列化学反应速率表示不正确的是( )
A. v(N2)=0.25 mol·L-1·min-1
B. v(H2)=0.75 mol·L-1·min-1
C. v(NH3)=1 mol·L-1·min-1
D. v(NH3)=0.5 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温条件下,可逆反应:2NO(g)+O2(g)![]() 2NO2(g)在体积固定的密闭容器中进行,达到平衡状态的标志的是( )
2NO2(g)在体积固定的密闭容器中进行,达到平衡状态的标志的是( )
①单位时间内生成n mol O2的同时生成2n mol NO2②单位时间内生成n mol O2的同时生成2n mol NO③用NO2、NO、O2表示的反应速率的比为2:2:1的状态④混合气体的颜色不再改变的状态⑤混合气体的密度不再改变的状态⑥混合气体的压强不再改变的状态⑦混合气体的平均相对分子质量不再改变的状态.
A. ①④⑥⑦ B. ②③⑤⑦ C. ①③④⑤ D. 全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A由碳、氢、氧三种元素组成,为研究A的结构,进行了如下实验:称取17.2gA在足量的氧气中燃烧,产物经过足量的浓硫酸后,浓硫酸增重10.8g;再通过足量的碱石灰,碱石灰增重35.2g。质谱图表明A的相对分子质量为86,A可以使溴的四氯化碳溶液褪色,且A能与等物质的量的NaHCO3溶液恰好完全反应,请回答:
(1)A的分子式为________。
(2)若A分子具有支链,则A的结构简式为________;其与NaHCO3溶液反应的化学反应方程式为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com