
| A. | BCl3 | B. | H2S | C. | NCl3 | D. | SF6 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | C2H6O | B. | CH3O | C. | C4H12O2 | D. | C5H10O4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电子数相同的粒子不一定属于同种元素 | |
| B. | 两个原子如果核外电子排布相同,一定属于同种元素 | |
| C. | 质子数相同,电子数也相同的两种粒子,不可能是一种分子和一种离子 | |
| D. | 所含质子数和电子数相等的粒子一定是原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4 C2H6 | B. | C2H4 C3H6 | C. | C2H4 C3H4 | D. | C2H6 C3H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④③①⑤ | B. | ②③⑤① | C. | ⑥③④① | D. | ⑥③①⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A的分子式为C2H4O3 | |
| B. | A的结构简式为HOCH2COOH | |
| C. | A分子中的官能团有两种 | |
| D. | 1 mol A与足量的单质Na反应时放出H2的物质的量为0.5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 滴加KI溶液时,KI被氧化,CuI是还原产物 | |
| B. | 通入SO2后,溶液变无色,体现SO2的还原性 | |
| C. | 上述实验条件下,物质的氧化性:Cu2+>I2>SO2 | |
| D. | 整个过程发生了复分解反应和氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
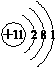 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com