
 某学习小组用乙醇与氢溴酸为原料制备溴乙烷.该反应发生的原理为:C2H5OH+HBr
某学习小组用乙醇与氢溴酸为原料制备溴乙烷.该反应发生的原理为:C2H5OH+HBr| △ |


科目:高中化学 来源: 题型:
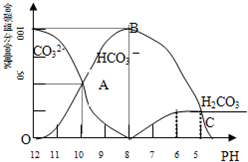 常温下在20mL0.1mol/LNa2CO3溶液中逐滴加入0.1mol/L HCl溶液40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如下图所示.回答下列问题:
常温下在20mL0.1mol/LNa2CO3溶液中逐滴加入0.1mol/L HCl溶液40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如下图所示.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:

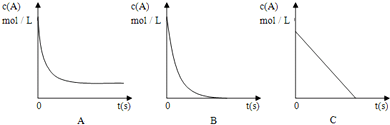
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等质量的Na2CO3和NaHCO3分别与足量的盐酸反应,Na2CO3生成的CO2多 |
| B、两者的水溶液都是呈现碱性,可以使无色的酚酞变红色 |
| C、加热时,Na2CO3难分解,但NaHCO3容易分解 |
| D、同温度下,Na2CO3在水中的溶解度比NaHCO3大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2.24L |
| B、4.48L |
| C、6.40L |
| D、12.8L |
查看答案和解析>>
科目:高中化学 来源: 题型:
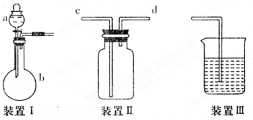 某实验小组利用如图所示装置完成有关实验.
某实验小组利用如图所示装置完成有关实验.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、K+、OH-、HCO3- |
| B、Cu2+、K+、SO42-、OH- |
| C、Na+、K+、Cl-、NO3- |
| D、Fe3+、Ca2+、SO42-、Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com