
| A、C2H4和C2H4O无论以何种比例混合,只要混合物总质量不变,完全燃烧时生成水的质量也不变 |
| B、分子式为C8H10且分子中有苯环的有机物共有3种 |
| C、汽油、柴油、植物油和甘油都是碳氢化合物 |
| D、溴苯分子中的所有原子都处在同一平面 |
 、邻二甲苯
、邻二甲苯 、对二甲苯
、对二甲苯 、间二甲苯
、间二甲苯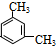 ,故B错误;
,故B错误;

 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4+、Na+、Ba2+、Cl- |
| B、Na+、I-、HCO3-、SO42- |
| C、K+、Cl-、SO32-、AlO2- |
| D、Na+、Mg2+、SO42-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
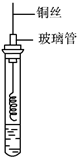 乙醇是一种重要的有机化工原料,它可以用玉米、薯类等为原料经发酵、蒸馏制成.乙醇和汽油经加工处理形成的车用燃料即乙醇汽油.
乙醇是一种重要的有机化工原料,它可以用玉米、薯类等为原料经发酵、蒸馏制成.乙醇和汽油经加工处理形成的车用燃料即乙醇汽油.查看答案和解析>>
科目:高中化学 来源: 题型:
A、用50mL8mol?L-1
| ||||||||
B、标准状况下,将1g
| ||||||||
C、向100mL3mol?L-1的稀硝酸中加入5.6g
| ||||||||
D、在5×107Pa、500℃和铁触媒催化的条件下,用
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol | B、2mol |
| C、2.5mol | D、5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| X | ||
| Y | ||
| Z |
| A、Y元素原子的外围电子排布为4s24p4 |
| B、Y元素在周期表的第三周期ⅥA族 |
| C、X元素所在周期中所含非金属元素最多 |
| D、Z元素的最高正价为+5价 |
查看答案和解析>>
科目:高中化学 来源: 题型:
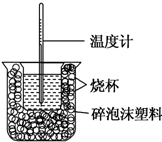 已知在稀溶液中,酸跟碱发生中和反应生成1mol水时的反应热叫做中和热.现利用如图装置进行中和热的测定,请回答下列问题:
已知在稀溶液中,酸跟碱发生中和反应生成1mol水时的反应热叫做中和热.现利用如图装置进行中和热的测定,请回答下列问题:| 反应物 | 起始温度t1/℃ | 终止温度t2/℃ | 中和热 |
| HCl+NaOH | 15.0 | 18.4 | △H1 |
| HCl+NH3?H2O | 15.0 | 18.1 | △H2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com