
在100ml含Cu2+、Al3+、NH4+、H+、NO3-的溶液中,逐滴加入2.5mol·L-1NaOH溶液,所加NaOH溶液的体积(ml)与产生沉淀的物质的量(mol)关系如下图所示。下列叙述正确的是

A.x-y=2×10-3mol B.原溶液的pH=2
C.原溶液中n(Cu2+)=0.025mol D.原溶液中c(NH4+)=7.5×10-3mol·L-1
科目:高中化学 来源:2017届河南省高三上学期第一次月考化学试卷(解析版) 题型:选择题
为提纯下列物质(括号中为杂质),所选除杂试剂和分离方法都正确的是( )
选项 | 待提纯的物质 | 除杂试剂 | 分离方法 |
A | NH3(H2O) | 浓硫酸 | 洗气 |
B | H2O(Br2) | CCl4 | 分液 |
C | KCl固体(I2) | KOH溶液 | 加热 |
D | 苯(苯酚) | 溴水 | 过滤 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高一上第二次月考化学卷(解析版) 题型:填空题
二氧化碳的捕捉和利用是我国能源领域的一个重要战略方向。
(1)用活性炭还原法可以处理汽车尾气中的氮氧化物,某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应C(s) + 2NO(g)  N2(g) + CO2(g) ΔH,在T1℃时,反应进行到不同时间测得各物质的量浓度如下:
N2(g) + CO2(g) ΔH,在T1℃时,反应进行到不同时间测得各物质的量浓度如下:
时间/min 浓度/(mol/L) | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 2.0 | 1.16 | 0.80 | 0.80 | 0.96 | 0.96 |
N2 | 0 | 0.42 | 0.60 | 0.60 | 0.72 | 0.72 |
CO2 | 0] | 0.42 | 0.60 | 0.60 | 0.72 | 0.72 |
①根据图表数据分析T1℃时,该反应在0-20min的平均反应速率v(N2)= mol·L-1·min-1;计算该反应的平衡常数K= 。
②30min后,只改变某一条件,根据上表的数据判断改变的条件可能是 (填字母代号)。
A.加入合适的催化剂 B.适当缩小容器的体积
C.通入一定量的NO D.加入一定量的活性炭
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则达到新平衡时NO的转化率 (填“升高”或“降低”),ΔH 0(填“>”或“<”).
(2)工业上用CO2和H2反应合成二甲醚。已知:
CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1=-49.1 kJ·mol-1
CH3OH(g)+H2O(g) △H1=-49.1 kJ·mol-1
2CH3OH(g) CH3OCH3(g)+H2O(g) △H2=-24.5 kJ·mol-1
CH3OCH3(g)+H2O(g) △H2=-24.5 kJ·mol-1
写出CO2(g)和H2(g)转化为CH3OCH3(g)和H2O(g)的热化学方程式 。
(3)二甲醚燃料电池具有能量转化率高、电量大的特点而被广泛应用,一种二甲醚氧气电池(电解质为KOH溶液)的负极反应式为:
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高一上第二次月考化学卷(解析版) 题型:选择题
海水中含有氯化镁,从海水中提取镁,可按如下步骤进行:①把贝壳制成石灰乳,②在引入海水的水渠中加石灰乳,沉降、过滤、洗涤沉淀物,③将沉淀物与盐酸反应,结晶过滤、干燥产物,④将得到的产物熔融后电解。关于提取镁,下列说法不正确的是( )
A.此法的优点之一是原料丰富
B.进行①②③步骤的目的是从海水中提取MgCl2
C.第④步电解时同时会产生氯气
D.以上提取镁的过程中涉及到的反应有分解反应、化合反应和置换反应
查看答案和解析>>
科目:高中化学 来源:2017届贵州省、贵阳一中高三上月考化学试卷(解析版) 题型:填空题
【化学——选修3:物质结构与性质】
X、Y、Z、W为前四周期元素且原子序数依次增大,X的电子层数等于核外电子数,Y元素基态原子核外未成对电子数为2且X与Y形成的化合物在常温下为常见的液体R,Z元素原子最外电子层上s、p电子数相等,W基态原子3d轨道的电子数是4s轨道电子数的3倍。请回答下列问题:
(1)Y基态原子的价电子排布图为 ,其第一电离能在同周期元素中由大到小排第 位。
(2)W的元素名称为 ,其基态原子核外有 种空间运动状态不同的电子。
(3)R的中心原子采取的杂化方式为 ,写出R的一个等电子体: 。(填化学式)。
(4)Z与Y在一定条件下可形成高硬度的化合物,该化合物的晶体类型为 ,其由Z、Y构成的最小环为 元环。
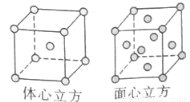
(5)W的单质在900℃以下为α型体心立方晶胞,910℃以上W转变为γ型面心立方晶胞,晶胞结构分别如图所示。两种晶体中距离最近的铁原子间距离相同。则在800℃和1000℃下,铁的密度之比为 。
查看答案和解析>>
科目:高中化学 来源:2017届贵州省、贵阳一中高三上月考化学试卷(解析版) 题型:选择题
常温下,下列各组离子一定能在指定溶液中大量共存的是
A.使pH试纸变蓝色的溶液中:K+、Al3+、NO3-、SO42-
B. =1×10-12mol·L-1的溶液中:NH4+、Cu2+、Cl-、SO42-
=1×10-12mol·L-1的溶液中:NH4+、Cu2+、Cl-、SO42-
C.有较多Fe3+的溶液中:Na+、SCN-、K+、Na+、CO32-
D.与Al反应能放出H2的溶液中:Fe2+、K+、NO3-、Cl-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江牡丹江高级中学高二9月月考化学卷(解析版) 题型:选择题
恒温恒压下,在容积可变的器皿中,反应2NO2 (g)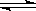 N2O4 (g)达到平衡后,再向容器内通入一定量NO2,又达到平衡时,N2O4的体积分数
N2O4 (g)达到平衡后,再向容器内通入一定量NO2,又达到平衡时,N2O4的体积分数
A.不变 B.增大 C.减小 D.无法判断
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江牡丹江高级中学高一9月月考化学卷(解析版) 题型:选择题
标准状况下V L氨气溶解在1 L水中(水的密度近似为1 g·mL-1),所得溶液的密度为ρ g·mL-1,质量分数为w,物质的量浓度为c mol·L-1 ,则下列关系中不正确的是
,则下列关系中不正确的是
A.w=17c/(1 000ρ) B.ρ=(17V+22 400)/(22.4+22.4V)
C.w=17V/(17V+22 400) D.c=1 000 Vρ/(17V+22 400)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一上9.18周考化学卷(解析版) 题型:计算题
在一定条件下,NO跟NH3可以发生反应生成N2和H2O。现有NO和NH3的混合物1mol,充分反应后所得产物中,若经还原得到的N2比经氧化得到的N2多1.4g。
(1)写出反应的化学方程式并标出电子转移的方向和数目。
(2)若以上反应进行完全,试计算原反应混合物中NO与NH3的物质的量可能各是多少。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com