
| 实验 次数 | 反应物及用量 | 溶 液 温 度 | ||
| t1 | t2 | |||
| 1 | 50mL0.55mol•L-1NaOH溶液 | 50mL.0.5mol•L-1HCl溶液 | 20℃ | 23.3℃ |
| 2 | 50mL0.55mol•L-1NaOH溶液 | 50mL.0.5mol•L-1HCl溶液 | 20℃ | 23.5℃ |
分析 (1)根据中和热测定的实验步骤选用需要的仪器,然后判断还缺少的仪器;
(2)①先求出2次反应的温度差的平均值,根据公式Q=cm△T来求出生成0.025mol的水放出热量,最后根据中和热的概念求出中和热;
②醋酸电离吸热.
解答 解:(1)中和热的测定过程中,需要用量筒量取酸溶液、碱溶液的体积,需要使用温度计测量温度,所以还缺少量筒、温度计;
故答案为:量筒、温度计;
(2)①第1次反应前后温度差为:3.3℃,第2次反应前后温度差为:3.5℃,平均温度差为3.4℃,50mL0.55mol•L-1NaOH溶液与50mL0.5mol•L-1HCl溶液混合,氢氧化钠过量,反应生成了0.025mol水,50mL0.5mol•L-1 盐酸、0.55mol•L-1NaOH溶液的质量和为:m=100mL×1g/mL=100g,c=4.18J/(g•℃),代入公式Q=cm△T得生成0.025mol的水放出热量Q=4.18J/(g•℃)×100g×3.4℃=1.4212kJ,即生成0.025mol的水放出热量1.4212kJ,所以生成1mol的水放出热量为1.4212kJ×$\frac{1mol}{0.025mol}$=-56.8kJ,即该实验测得的中和热△H=-56.8kJ•mol-1;
故答案为:-56.8kJ•mol-1;
②醋酸电离过程为吸热过程,所以用醋酸代替HCl做实验,反应放出的热量偏小,但△H偏大;
故答案为:>.
点评 本题考查热了中和热的测定方法及反应热的计算,题目难度中等,注意理解中和热测定原理以及测定反应热的误差等问题,试题培养了学生灵活应用所学知识的能力.


科目:高中化学 来源: 题型:选择题
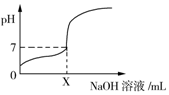 常温下,用0.1mol/L的NaOH溶液滴定20mL同浓度的一元弱酸HA,滴定过程中溶液pH随NaOH溶液体积变化曲线如图所示(忽略中和热效应),下列说法正确的是( )
常温下,用0.1mol/L的NaOH溶液滴定20mL同浓度的一元弱酸HA,滴定过程中溶液pH随NaOH溶液体积变化曲线如图所示(忽略中和热效应),下列说法正确的是( )| A. | X=20 | |
| B. | HA溶液加水稀释后,溶液中$\frac{c(HA)}{{c({A^-})}}$的值减小 | |
| C. | 0.1 mol/L的NaOH溶液中,由水电离出的c(OH-)=0.1 mol/L | |
| D. | 加入NaOH溶液体积为X mL时,溶液中c(A-)=0.05 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 泡沫灭火器中用的是苏打和硫酸铝 | |
| B. | 沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强 | |
| C. | 理想的催化剂可以大幅度提高目标产物在最终产物的比率 | |
| D. | Na与H2O的反应是熵减的放热反应,该反应能自发进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含16g氧原子的二氧化硅晶体中含有的δ键数目为2NA | |
| B. | 1mol甲基(-CH3)所含电子数为9NA | |
| C. | 12克石墨中含有的共价键数目为1.5NA | |
| D. | 2molSO2和1molO2在一定条件下反应所得混合气体分子数等于2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 糖类、油脂、蛋白质的水解产物都是非电解质 | |
| B. | 蔗糖、麦芽糖的分子式均为C12H22O11,二者互为同分异构体 | |
| C. | 甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应 | |
| D. | 乙醇、乙酸分子中均含有官能团-OH,所以均能与NaOH溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
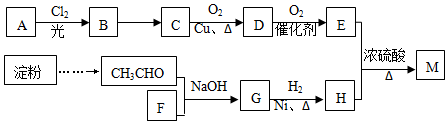
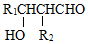
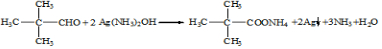 ;
;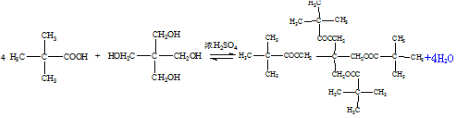 ;
;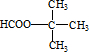 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2-氯丁烷与氢氧化钠、乙醇在加热条件下的消去反应 | |
| B. | 乙烯通入溴水中的加成反应 | |
| C. | 灼热的铜丝插入足量乙醇中的氧化反应 | |
| D. | 苯酚与足量的氢气在一定条件下的加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.12 g铁与足量浓硫酸反应 | |
| B. | 0.12g镁与足量盐酸反应 | |
| C. | 0.02mol钠与足量水反应 | |
| D. | 0.01mol铝与足量氢氧化钠溶液反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com