
分析 依据n=$\frac{m}{M}$=$\frac{N}{N{\;}_{A}}$=$\frac{V}{Vm}$结合物质的组成结构解答.
解答 解:①1个水分子含有2个H,则1molH2O含有2molH,个数为:2NA;
故答案为:2NA;
②N=nNA=0.25×NA=0.25 NA,
故答案为:0.25 NA;
③N=nNA=0.3×NA=0.3 NA,
故答案为:0.3 NA;
④0.5molHCl占有的体积V=0.5mol×22.4L/mol=11.2L;
故答案为:11.2L;
⑤33.6LH2的物质的量是:$\frac{33.6L}{22.4L/mol}$=1.5mol;
故答案为:1.5mol;
⑥二氧化碳的相对分子质量为44,则其摩尔质量为44g/mol;
故答案为:44g/mol;
⑦22gCO2的物质的量为:$\frac{22g}{44g/mol}$=0.5mol;
故答案为:0.5mol.
点评 本题考查了物质的量有关计算,明确以物质的量为核心计算公式是解题关键,注意相关物质的结构组成,题目难度不大,侧重考查学生对基础知识掌握熟练程度.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
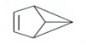 盆烯是近年来运用立体空间化学制造出来的空间单烯烃,因其分子形似瓦盆,故称为盆烯,其结构简式如图所示.下列关于盆烯的说法中正确的是( )
盆烯是近年来运用立体空间化学制造出来的空间单烯烃,因其分子形似瓦盆,故称为盆烯,其结构简式如图所示.下列关于盆烯的说法中正确的是( )| A. | 分子式为C6H8 | |
| B. | 是乙烯的一种同系物 | |
| C. | 在一定条件下可以发生加成、氧化反应 | |
| D. | 1 mol盆烯完全燃烧需消耗6.5molO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 COOCH2CH2CH(OH3)2.合成路线如下:
COOCH2CH2CH(OH3)2.合成路线如下: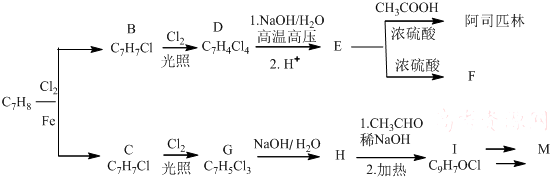
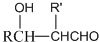 $\stackrel{加热}{→}$H2O+
$\stackrel{加热}{→}$H2O+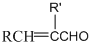
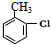 ,由H生成I的第二步反应的反应类型是消去反应.
,由H生成I的第二步反应的反应类型是消去反应.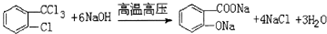 .E→F
.E→F .
.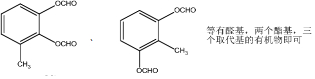 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知一个H2分子的体积是VL,则H2的摩尔体积是VNA L/mol | |
| B. | 肼(N2H4),熔点20℃,沸点113.5℃,标况下,11.2L肼的原子数小于3NA | |
| C. | 25℃、101KPa下,16gNH2-含有10NA个电子 | |
| D. | 标况下,4gH2、11.2LO2、1molSO3中O2体积最小 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com