
A、B、C、D四种物质均为下列离子组成的可溶性化合物,组成这四种物质的离子(离子不能重复组合)有:
| 阳离子 | Na+、Al3+、Ba2+、NH4+ |
| 阴离子 | Cl-、OH-、CO32-、SO42- |
分别取四种物质进行实验,实验结果如下:
①A、D溶液呈碱性,B呈酸性,C呈中性
②A溶液与B溶液反应生成白色沉淀,再加过量A,沉淀量减少,但不会完全消失
③A溶液与D溶液混合并加热有气体生成,该气体能使湿润的红色石蕊试纸变蓝
回答下列问题:
(1)A的化学式是_________,用电子式表示C的形成过程:________________ 。
(2)向A溶液中通入适量CO2,使生成的沉淀恰好溶解,所得溶液中各离子物质的量浓度由大到小的顺序是:________________________ 。
(3)写出③的离子方程式_______________________________________________ 。
(4)简述D溶液呈碱性的理由___________________________________________ 。
【知识点】离子共存问题;盐类水解的应用 B4 H3 H6
【答案解析】(1) Ba(OH)2

(2) c(HCO3﹣)>c(Ba2+)>c(OH﹣)>c(H+)>c(CO32﹣)
(3) Ba2++CO32﹣+2NH4++2OH﹣ 2NH3↑+2H2O+BaCO3↓
2NH3↑+2H2O+BaCO3↓
(4) NH4+的水解程度小于CO32﹣的水解程度
解析:根据A溶液与D溶液混合并加热有气体生成,该气体能使湿润的红色石蕊试液变蓝,气体为氨气,再由A、D溶液呈碱性,B呈酸性,C呈中性,A溶液与B溶液反应生成白色沉淀,再加过量A,沉淀量减少,但不会完全消失,则A为Ba(OH)2,B为强酸弱碱盐,则B为Al2(SO4)2,C为强酸强碱盐,则C为NaCl,D为弱酸弱碱盐,则D为(NH4)2CO3。
(1)A为Ba(OH)2;C为NaCl,其形成过程为 ;
;
(2)向A溶液中通入适量CO2,使生成的沉淀恰好溶解,溶液的溶质为Ba(HCO3)2,由化学式及电离可知c(HCO3-)>c(Ba2+),再由水解显碱性可知c(OH-)>c(H+),电离产生极少的CO32-,即离子物质的量浓度由大到小的顺序为c(HCO3-)>c(Ba2+)>c(OH-)>c(H+)>c(CO32-);
(3)③为Ba(OH)2与(NH4)2CO3的反应,其离子反应为Ba2++CO32-+2NH4++2OH- 2NH3↑+2H2O+BaCO3↓,
2NH3↑+2H2O+BaCO3↓,
(4)(NH4)2CO3溶液显碱性,是因NH4+的水解程度小于CO32-的水解程度。
【思路点拨】本题考查了物质的推断、离子的共存、离子浓度大小的比较、水解、离子反应等知识,综合性较强,难度较大,需要学生在推断时综合考虑信息的利用,对学生能力要求较高。


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源: 题型:
三氟化氮(NF3)是一种新型电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3。下列有关说法正确的是
A.反应中NF3是氧化剂,H2O是还原剂
B.反应中被氧化与被还原的原子物质的量之比为2:1
C.若反应中生成0.2 mol HNO3,则反应共转移0.2 mol e-
D. NF3在潮湿空气中泄漏会产生白雾、红棕色气体等现象
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列各溶液中,离子一定能大量共存的是: ( )
A.pH=11的溶液中:CO32-、Na+、AlO2-、NO3-
B.含有0.1mol·L-1Fe3+的溶液中:K+、Mg2+、I-、NO3-
C.无色溶液中:K+、Na+、MnO4-、SO42-
D.室温下,pH=1的溶液中:Na+、Fe2+、NO3-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
硫、氯及其化合物由广泛的用途。
(1)“氯氧化法”是指在碱性条件下用Cl2将废水中的CN-氧化成无毒的物质,CN-被氧化后的产物为_______________________(填化学式)。
(2)“氯胺(NH2Cl)消毒法”是在用液氯处理自来水的同时通入少量氨气,发生反应:Cl2+NH3=NH2Cl+HCl,生成的NH2Cl能部分水解生成强氧化性的物质,起消毒杀菌的作用。氯胺能用于消毒杀菌的原因是___________________(用化学方程式表示)。
(3)如图所示装置和药品可用来制备Na2S2O3.

①H2CO3、H2S、H2SO3三种酸的酸性由强到弱的顺序为_________________.
②配平广口瓶中生成Na2S2O3反应的化学方程式:
()SO2+()Na2S+()Na2CO3——()Na2S2O3+()CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
碱式碳酸盐A可用作胃药,其组成可表示为Al2Mg6(OH)x(CO3)y·zH2O。某校化学兴趣小组欲测定其化学式,实验设计如下:
实验Ⅰ:称取一定质量的A,加热分解至恒重。
实验Ⅱ:称取一定质量的A,与足量的酸反应,测量生成CO2气体的质量。
可供选择的仪器和药品如图所示:(酸溶液限选6 mol·L-1盐酸或6 mol·L-1硫酸,其他试剂任选)
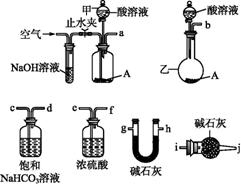
回答下列问题:
(1)仪器乙的名称为 。
(2)请选择必要的装置完成实验Ⅱ,正确的连接顺序为 (按气流方向,用接口字母表示);选用的酸溶液是 。
(3)有人提出不采用实验Ⅰ,可在实验Ⅱ结束后,在A完全反应后所得溶液中滴加足量的氨水,用无灰滤纸过滤,用蒸馏水洗涤反应容器2~3次,将洗涤液过滤,洗涤沉淀2~3次,将附着沉淀的滤纸放到坩埚中加热分解至恒重。判断沉淀已洗涤干净的方法是 ,实际上 未采用该方案的原因是不符合实验设计的 (填字母编号)原则。
未采用该方案的原因是不符合实验设计的 (填字母编号)原则。
A.科 学性 B.安全性
学性 B.安全性
C.可行性 D.简约性
(4)x与y的关系式是 (用等式表示)。
(5)通过实验Ⅰ的相关数据,经计算可得A的摩尔质量为602.0 g·mol-1。实验Ⅱ中称得样品A的质量为9.030 g,与足量酸完全反应后,CO2吸收装置增重0.660 g,则A的化学式为  。
。 
查看答案和解析>>
科目:高中化学 来源: 题型:
氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液与“另一物质”在40~50 ℃时反应可生成它。CuH具有的性质有:不稳定,易分解,在氯气中能燃烧;与稀盐酸反应能生成气体;Cu+在酸性条件下发生的反应是2Cu+ Cu2++Cu。
Cu2++Cu。
根据以上信 息,结合自己所掌握的化学知识,回答下列问题:
息,结合自己所掌握的化学知识,回答下列问题:
(1)用CuSO4溶液与“另一物质”制CuH的反应中,用氧化还原观点分析,这“另一物质”在反应中作 (填“氧化剂”或“还原剂”)。
(2)写出CuH在氯气中燃烧的化学反应方程式: 。
(3)CuH溶解在稀盐酸中生成的气体是 (填化学式)。
(4)如果把CuH溶解在足量的稀硝酸中生成的气体只有NO,请写出CuH溶解在足量稀硝酸中反应的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
维生素C的结构简式为
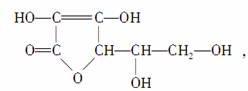 丁香油酚的结构简式为:
丁香油酚的结构简式为:
 下列关于两者的说法正确的是( )
下列关于两者的说法正确的是( )
A.均含酯基 B.均含醇羟基和酚羟基
C.均含碳碳双键 D.均为芳香化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝,在上述溶液中加入足量的亚硫酸钠溶液,蓝色逐渐消失。下列判断不正确的是( )
A.氧化性:ClO –>I2>SO42– B.漂白粉溶液可使淀粉碘化钾试纸变蓝
C.向氯水中加入亚硫酸钠溶液,氯水褪色 D.次氯酸钠可以与亚硫酸钠共存
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com