
| A. | 101kPa时,能表示H2燃烧热的热化学方程式为:H2(g)+Cl2(g)=2HCl(g);△H=-183kJ/mol | |
| B. | 向Mg(OH)2悬浊液中滴入饱和NH4Cl溶液,沉淀溶解,其离子方程式为:Mg(OH)2+2H+═Mg2++2H2O | |
| C. | 电解精炼铜的阳极反应式为:Cu2++2e-=Cu | |
| D. | 硫代硫酸钠溶液中加入稀硫酸变浑浊:S2O32-+2H+=S↓+SO2↑+H2O |
分析 A.燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量;
B.漏掉氨根离子与氢氧根离子的反应;
C.阳极发生氧化反应;
D.硫代硫酸钠溶液中加入稀硫酸变浑浊反应生成硫单质和二氧化硫和水.
解答 解:A.氢气在氯气中燃烧生成的不是氧化物,所以H2(g)+Cl2(g)=2HCl(g);△H=-183kJ/mol不是氢气燃烧热的热化学方程式,故A错误;
B.向Mg(OH)2悬浊液中滴入饱和NH4Cl溶液,沉淀溶解,其离子方程式为Mg(OH)2+2NH4+=2Mg2++2NH3↑+2H2O,故B错误;
C.电解精炼铜的阳极反应式为:Cu-2e-=Cu2+,故C错误;
D.硫代硫酸钠溶液中加入稀硫酸变浑浊,离子方程式:S2O32-+2H+=S↓+SO2↑+H2O,故D正确;
故选:D.
点评 本题考查了离子方程式的书写,明确反应实质是解题关键,注意化学式的拆分及离子方程式应遵循原子个数守恒、电荷数守恒规律,题目难度不大.


科目:高中化学 来源: 题型:多选题
| A. | 2NaHCO3═Na2CO3+CO2↑+H2O | B. | MnO2+4 HCl(浓)═MnCl2+Cl2↑+2 H2O | ||
| C. | 2 H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2 H2O+O2↑ | D. | Na2CO3+CaCl2═CaCO3↓+2NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一个“双重结构”的分子实际上是两个分子 | |
| B. | 该分子原子间都以共价键相连接 | |
| C. | 该物质是一种新的化合物 | |
| D. | 该物质的相对分子质量为2400 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
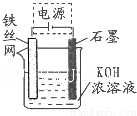 铁及其化合物在生产、生活中有广泛应用.请回答下列问题:
铁及其化合物在生产、生活中有广泛应用.请回答下列问题:| 温度/℃ | 1000 | 1115 | 1300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg+2H2O═Mg(OH)2+H2↑ | B. | 2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑ | ||
| C. | 2F2+2H2O═O2+4HF | D. | 3NO2+H2O═2HNO3+NO |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ;Y离子的电子式为Al3+.
;Y离子的电子式为Al3+.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com