
已知A、B、C、D之间的转化关系如图所示。下列说法正确的是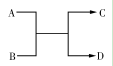
A.若A为Fe,D为氢气,则B一定为酸
B.若A、D为化合物,B为水,则C一定是气体单质
C.若A、B、C、D均为化合物,该反应一定属于复分解反应
D.若A、B、C、D均为10电子微粒,且C是可使湿润的红色石蕊试纸变蓝的气体,则D在常温下一定呈液态
科目:高中化学 来源: 题型:实验题
下图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略)。
(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关的离子反应方程式为 ;
装置B中饱和食盐水的作用是_________;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象 ;
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III依次放入 ;
| | a | b | c | d |
| I | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| II | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| III | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
为探究某铁碳合金与浓硫酸在加热条件下的反应的部分产物并测定铁碳合金中铁元素的质量分数,某化学活动小组设计了下图所示的实验装置,并完成以下实验探究。
|
|

 (1)往圆底烧瓶中加入m g铁碳合金,并滴入过量浓硫酸,未点燃酒精灯前,A、B均无明显现象,其原因是:①常温下,Fe在浓硫酸中钝化;② 。
(1)往圆底烧瓶中加入m g铁碳合金,并滴入过量浓硫酸,未点燃酒精灯前,A、B均无明显现象,其原因是:①常温下,Fe在浓硫酸中钝化;② 。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
该学习小组通过查阅资料发现用KClO3和浓盐酸也可以制备氯气。为此该小组利用下图装置在实验室制取Cl2并探究其有关性质:
(1)装置A中存在一处错误,改正这处错误: 。
(2)写出装置A中发生反应的化学方程式: 。
(3)为了除去氯气中的氯化氢,需要在.A、B之间装置中添加装置E,装置E中所盛装的试剂为 。为了探究使有色布条褪色的是氯气还是氯气与水反应的生成物,需要在整套装置中添加装置E,其中加入浓硫酸,装置E在整套装置中的添加位置为 (选填序号)。
a A、B之间 b.B、C之间
c.C、D之间 d.D之后
(4)取下集气瓶B,将铁丝加热至红热状态,伸入到集气瓶B中,可以观察到的现象是 ,能检验该反应产物中铁元素的价态的试剂 (选填序号,多选)。
a.氯水 b.蒸馏水和铁粉
c.蒸馏水和氢氧化钠溶液 d.蒸馏水和KSCN溶液
(5)另外一个化学学习小组就环境保护方面指出了上述装置的缺陷?并给出了改进措施。该改进措施是: 。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
为了证明在实验室制备Cl2的过程中会有水蒸气和HCl挥发出来,甲同学设计了如图所示的实验装置,按要求回答问题: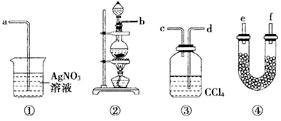
(1)请根据甲同学的意图,连接相应的装置,接口顺序:b接 , 接 , 接
。
(2)U形管中所盛试剂的化学式为 。
(3)装置③中CCl4的作用是 。
(4)乙同学认为甲同学实验有缺陷,不能证明最终通入AgNO3溶液中的气体只有一种,为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之间再加装置⑤。你认为装置⑤应加在 之间(填装置序号)。瓶中可以放入 。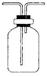
(5)丙同学看到甲同学设计的装置后提出无需多加装置,只需将原来烧杯中的AgNO3溶液换成其他溶液。你认为可将溶液换成 ,如果观察到 现象,则证明制Cl2时有HCl挥发出来。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
甲、乙、丙、X是中学化学中常见的4种物质,其转化关系符合下图。其中甲和X不可能是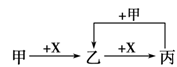
A.甲为C、X为O2
B.甲为Fe、X为Cl2
C.甲为SO2、X为NH3·H2O
D.甲为AlCl3溶液、X为NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
中学常见物质A、B、C、D、E、X,存在下图转化关系(部分生成物和反应条件略去)。下列推断不正确的是 
A.若D是一种白色沉淀,在空气中最终变为红褐色,则A可能是铁
B.若D是一种强碱,则A、B、C均可与X反应生成D
C.若D为NaCl,且A可与C反应生成B,则E可能是CO2
D.若D是一种强酸,则A既可以是单质,也可以是化合物,且D可与铜反应生成B或C
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知X为一种常见酸的浓溶液,能使蔗糖粉末变黑。A与X反应的转化关系如图所示,其中反应条件及部分产物均已略去,则下列有关说法正确的是( )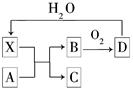
| A.X使蔗糖变黑的现象主要体现了X的强氧化性 |
| B.若A为铁,则足量A与X在室温下即可完全反应 |
| C.若A为碳单质,则将C通入少量的澄清石灰水中,一定可看到白色沉淀 |
| D.工业上,B转化为D的反应条件为高温、常压、使用催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下表各组物质中,满足如图物质一步转化关系的选项是( )
| 选项 | X | Y | Z |
| A | Na | NaOH | NaHCO3 |
| B | Cu | CuSO4 | Cu(OH)2 |
| C | C | CO | CO2 |
| D | Si | SiO2 | H2SiO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com