

分析 (1)仪器a为球形干燥管,作用是干燥氧气和氨气的混合气体,应选用碱性干燥剂;
(2)移去酒精灯,Cr2O3固体保持红热说明反应放热;
装置C中发生反应的化学反应是氨气的催化氧化反应生成一氧化氮和水;
(3)无水氯化钙是常用的干燥剂,同时氯化钙可以与NH3反应生成八氨合氯化钙;氢氧化钠溶液可以吸收酸性气体;
(4)一氧化氮与空气中的氧气反应生成二氧化氮;
(5)二氧化氮气体与水反应生成硝酸,硝酸遇到石蕊试液变红色;
(6)根据氢氧化钠的物质的量计算硝酸的浓度.
解答 解:(1)仪器a为球形干燥管,作用是干燥氧气和氨气的混合气体,应选用碱性干燥剂碱石灰,故答案为:球形干燥管;碱石灰;
(2)装置C中发生反应的化学反应是氨气的催化氧化反应生成一氧化氮和水,反应的化学方程式为:4NH3+5O2$\frac{\underline{\;Cr_{2}O_{3}\;}}{△}$4NO+6H2O;
移去酒精灯,Cr2O3固体保持红热说明反应放热,
故答案为:该反应为放热反应;4NH3+5O2$\frac{\underline{\;Cr_{2}O_{3}\;}}{△}$4NO+6H2O;
(3)氯化钙可以与NH3反应生成八氨合氯化钙,无水氯化钙是常用的干燥剂,故可以吸收氨气和水蒸气;装置G中盛放的是氢氧化钠溶液,可以吸收尾气,防治污染环境;
故答案为:除去氨气和水蒸气;吸收尾气;
(4)无色的一氧化氮与空气中的氧气反应生成红棕色的二氧化氮,故答案为:气体变为红棕色;
(5)二氧化氮气体与水反应生成硝酸,硝酸遇到石蕊试液变红色,故证明有HNO3生成的操作是:取少量F中的液体于试管中,滴加几滴紫色石蕊试液,溶液变红,证明有HNO3生产,
故答案为:取少量F中的液体于试管中,滴加几滴紫色石蕊试液,溶液变红,证明有HNO3生产;
(6)反应制得的硝酸的浓度为$\frac{0.100mol×25ml}{20ml}$×$\frac{1000ml}{20ml}$=6.25mol/L,故答案为:6.25.
点评 本题以氨氧化法制取硝酸为载体考查物质制备的实验探究和物质性质的分析应用,题目难度中等.


 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案科目:高中化学 来源: 题型:选择题
| A. | 将氯气溶于水,须通入倒置并边缘没入水中的漏斗 | |
| B. | 粉碎结块的硝酸铵,可将药品放入研体中轻轻敲碎 | |
| C. | 洗涤做过银镜反应的试管,先用浓硝酸洗涤,再用自来水冲洗 | |
| D. | 玻璃导管与橡皮导管连接,可使玻璃导管蘸水后边旋转边插入橡皮导管 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
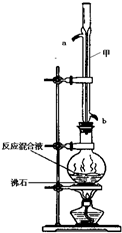 苯甲酸甲酯是一种重要的工业原料,某化学小组采用如图装置,以苯甲酸、甲醇为原料制取苯甲酸甲酯.有关物质的物理性质见下表所示:
苯甲酸甲酯是一种重要的工业原料,某化学小组采用如图装置,以苯甲酸、甲醇为原料制取苯甲酸甲酯.有关物质的物理性质见下表所示:| 苯甲酸 | 甲醇 | 苯甲酸甲酯 | |
| 熔点/℃ | 122.4 | -97 | -12.3 |
| 沸点/℃ | 249 | 64.3 | 199.6 |
| 密度/g.cm-3 | 1.2659 | 0.792 | 1.0888 |
| 水溶性 | 微溶 | 互溶 | 不溶 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t1~t2 | t3~t4 | t4~t5 | t6~t7 |
| K1 | K2 | K3 | K4 |

| 物质 | CO2 | CH4 | CO | H2 |
| 浓度(mol•L-1) | 1 | 1 | 1 | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 弱酸化学式 | H2SO3 | H2CO3 |
| 电离常数(25℃) | Ka1=1.3×10-2 Ka2=6.3×10-8 | Ka1=4.2×10-7 Ka2=5.6×10-11 |
| A. | c(HCO3-)<c(CO32-) | |
| B. | 两溶液都能使酸性高锰酸钾溶液褪色 | |
| C. | c(HCO3-)>c(HSO3-) | |
| D. | c(CO32-)+c(HCO3-)=c(SO32-)+c(HSO3-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 醋酸的电离度 | B. | 溶液的导电性 | ||
| C. | 溶液的c(OH-) | D. | 溶液中$\frac{[C{H}_{3}COO].[{H}^{+}]}{[C{H}_{3}COOH]}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| Z | M | R | Q | |
| 原子半径/nm | 0.186 | 0.074 | 0.099 | 0.143 |
| 主要化合价 | -2 | -1,+7 | +3 |
| A. | X与M形成的化合物中含有离子键 | |
| B. | Z、M、Q三种元素的简单离子的半径:M>Z>Q | |
| C. | Y与R形成的化合物中R呈正价,说明Y的非金属性比R强 | |
| D. | 在元素周期表中,Q位于金属与非金属的交界处,可以作半导体材料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com