



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����2H��18O����ɵ�ˮ11 g��������������Ϊ4NA |
| B��1 mol CO2�к��еĹ��ۼ�����ĿΪ2NA |
| C����0.1 mol��L��1 K2CO3��Һ�У���������Ŀ����0.1NA |
| D��NO2��H2O��Ӧÿ����2 mol HNO3ʱת�Ƶĵ�����ĿΪ2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��110��ʱ������Ӧǰ������干NA�����ӣ���Ӧ��õ�0.65NA��������� |
| B��110��ʱ��2NA��H2S����������ǡ�÷�Ӧ�꣬�����������Է�������Ϊ20 |
| C��0��ʱ��������2.24L�̼������壬��ת�Ƶ�����Ϊ0.8NA |
| D�����õ�������������NA��ԭ�ӣ���μӷ�Ӧ�ķ�Ӧ�������NA�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��11.2 L N2����������Ϊ0.5NA |
| B�������£�16 g CH4�й��õ��ӶԵ���ĿΪ4NA |
| C��һ���¶��£�1 mol FeCl3ˮ������NA��Fe(OH)3������� |
| D���ڷ�ӦH2O2��Cl2=2HCl��O2�У�ÿ����32 g������ת��4NA������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���٢� | B���ۢ� | C���ڢ� | D���ݢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����״���£�11��2L�����������ķ�����Ϊ0��5NA |
| B��28g��ϩ�������õ��Ӷ���ĿΪ4NA |
| C����״���£�11��2 L���ȼ�������������Ϊ0��5 NA |
| D��������ϩ����ϩ����ϩ�Ļ�����干14g����ԭ����Ϊ3NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��1mol�״��к���C��H������ĿΪ4NA |
| B��25�棬pH��13��NaOH��Һ�к���OH������ĿΪ0.1NA |
| C��Na2O2������H2O��Ӧ����0.2mol O2��ת�Ƶ��ӵ���ĿΪ0.4NA |
| D����״���£�2.24 L���麬�з��ӵ���ĿΪ0.1 NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

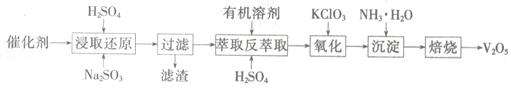
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��������Һ�����ʵ���Ũ�ȣ�c��1 mol��L��1 |
| B��������Һ�к���NA��HCl���� |
| C��36.5 g HCl����ռ�е����Ϊ22.4 L |
| D��������Һ������������W��36.5 c/(1 000��) |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com