
| 15 |
| 16 |
| ||
| △ |
| ||
| 1-x+3-3x+2x |
| 1+3 |
| 15 |
| 16 |
| 0.125 |
| 1 |
| ||
| 12.6t |
| 50% |
| 0.03 |
| 0.1 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
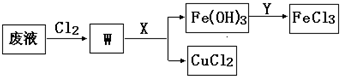 我国是世界上发现和使用铜及铜器最早的国家之一,直到现在铜及其化合物在工农业生产中仍然有着广泛的应用.
我国是世界上发现和使用铜及铜器最早的国家之一,直到现在铜及其化合物在工农业生产中仍然有着广泛的应用.查看答案和解析>>
科目:高中化学 来源: 题型:
| 族 周期 |
IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、15.6 g Na2O2与过量CO2反应时,转移电子数为0.4NA |
| B、5.6 g Fe与过量硫粉反应,转移电子数为0.3NA |
| C、3.1 g白磷与红磷的混合物中所含磷原子数为0.1NA |
| D、某温度时,pH=6的纯水中含10-6NA个OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 将0.050mol SO2和0.030mol O2放入容积为1L的密闭容器中,在一定条件下发生如下反应:2SO2(g)+O2(g)?2SO3(g),△H=-196.64kJ/mol.
将0.050mol SO2和0.030mol O2放入容积为1L的密闭容器中,在一定条件下发生如下反应:2SO2(g)+O2(g)?2SO3(g),△H=-196.64kJ/mol.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH<7,且c(CH3COO-)>c(H+)>c(Na+)>c(OH-) |
| B、pH>7,且c(OH-)>c(Na+)>c(H+)>c(CH3COO-) |
| C、pH>7,且c(Na+)+c(H+)=c(OH-)+c(CH3COO-) |
| D、pH=7,且c(CH3COO-)=c(Na+)>c(H+)=c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| n |
| 2 |
| 3n |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 常温下,用0.1mol/L CH3COOH溶液滴定20mL O.1mol/L NaOH溶液的滴定曲线如图所示,则在混合后的溶液中下列粒子浓度的关系式干不正确的是(忽略溶液混合时体积变化)( )
常温下,用0.1mol/L CH3COOH溶液滴定20mL O.1mol/L NaOH溶液的滴定曲线如图所示,则在混合后的溶液中下列粒子浓度的关系式干不正确的是(忽略溶液混合时体积变化)( )| A、pH=8时:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| B、a点时:c(OH-)=c(H+)+c(CH3COO-)+c(CH3COOH) |
| C、PH=7时:c(CH3COO-)+c(H+)=c(Na+)+c(OH-) |
| D、b点时:c(CH3COO-)+c(CH3COOH)=0.05mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com