
下列叙述中正确的是
A.同温同压下,相同体积的物质,所含的粒子数必相等
B.任何条件下,等质量的乙烯和一氧化碳所含的分子数必相等
C.1 L一氧化碳气体的质量一定比1 L氧气的质量小
D.等体积、等物质的量浓度的强酸中所含的H+数目一定相等
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2016届浙江省新安江校区高三上学期第二次模拟化学试卷(解析版) 题型:选择题
化学与生产、生活、社会密切相关。下列有关说法中正确的是
A.明矾水解时产生具有吸附性的胶体粒子,可以用于饮用水的杀菌消毒
B.SiO2制成的玻璃纤维,由于导电能力强而被用于制造通讯光缆
C.鼓励汽车、家电“以旧换新”,可减少环境污染,发展循环经济,促进节能减排
D.焰火“脚印”、“笑脸”使北京奥运会开幕式更加辉煌、浪漫,这与高中化学中“焰色反应”的知识相关,焰色反应是化学变化
查看答案和解析>>
科目:高中化学 来源:2016届四川省高三上学期10月月考化学试卷(解析版) 题型:选择题
将Na2O2逐渐加入到含有H+、Mg2+、Al3+、NH4+的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入的Na2O2物质的量(mol)的关系如图所示,则原溶液中的Mg2+、Al3+、NH4+物质的量分别
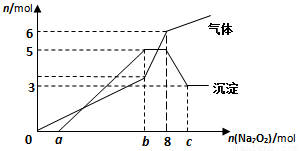
A. 2 mol、3 mol、6 mol B. 3 mol、2 mol、6mol
C. 2 mol、3 mol、4 mol D. 3 mol、2 mol、2 mol
查看答案和解析>>
科目:高中化学 来源:2016届河南省英文学校高三上学期期中测试化学试卷(解析版) 题型:实验题
(14分)某校化学实验兴趣小组在“探究卤索单质的氧化性”的系列实验中发现:在足量的稀氯化亚铁溶液中,加入l~2滴溴水,振荡后溶液呈黄色。
提出问题 Fe3+、Br2谁的氧化性更强?
(1)猜 想:①甲同学认为氧化性:Fe3+>Br2,故上述实验现象不是发生化学反应所致,则溶液呈黄色是含 (填化学式,下同)所致。
②乙同学认为氧化性:Br2>Fe3+,故上述实验现象是发生化学反应所致,则溶液呈黄色是含 所致。
(2)设计实验并验证
丙同学为验证乙同学的观点,选用下列某些试剂设计出两种方案进行实验,并通过观察实验现象,证明了乙同学的观点确实是正确的。
供选用的试剂:a.酚酞试液;b.CCl4;c.无水酒精;d.KSCN溶液。
请你在下表中写出丙同学选用的试剂及实验中观察到的现象。(试剂填序号)
选用试剂 | 实验现象 | |
方案1 | ||
方案2 |
(3)结论:氧化性:Br2>Fe3+。故在足量的稀氯化亚铁溶液中,加入l~2滴溴水,溶液呈黄色所发生的离子反应方程式为 。
(4)实验后的思考
①根据上述实验推测,若在溴化亚铁溶液中通入氯气,首先被氧化的离子是: (填离子的化学式)。
②在100 mL FeBr2溶液中通入2.24 L Cl2(标准状况),溶液中有1/2的Br-被氧气成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为 。
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省绥化市高三上学期期中测试化学试卷(解析版) 题型:选择题
下列物质与其用途完全符合的有
①Na2CO3—制玻璃;②SiO2—太阳能电池;③AgI—人工降雨;
④NaCl—制纯碱;⑤Al2O3—焊接钢轨;⑥NaClO—消毒剂、漂白织物
⑦Fe2O3—红色油漆或涂料⑧MgO—耐火材料
A.4个 B.5个 C.6个 D.7个
查看答案和解析>>
科目:高中化学 来源:2016届湖南省益阳市高三上学期第二次模拟测试化学试卷(解析版) 题型:选择题
在一密闭容器中有HCHO、H2、O2共26.5 g,用电火花引燃烧,使其完全燃烧,再将燃烧后的气体用Na2O2充分吸收,Na2O2 增重10.5 g,则原混合气体中O2的物质的量是
A.0.5 mol B.0.25 mol C.0.27 mol D.0.52 mol
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列反应不属于取代反应的是
A.淀粉水解制葡萄糖
B.石油裂解制丙烯
C.乙醇与乙酸反应制乙酸乙酯
D.油脂与浓NaOH反应制高级脂肪酸钠
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高三上学期第一次月考化学试卷(解析版) 题型:填空题
(10分)四种短周期元素W、X、Y、Z,原子序数依次增大,请结合表中信息回答下列问题。
W | X | Y | Z | |
结构 或性质 | 最高价氧化物对应的水 化物与其气态氢化物反 应得到离子化合物 | 焰色反应呈黄色 | 在同周期主族元素形成的简单离子中,离子半径最小 | 最高正价与最 低负价之和为6 |
(1)W元素和氢可形成离子化合物,其电子式为 。
(2)Y元素和Z元素可形成YZ3化合物,可用于净水剂,净水原理 (用离子方程式表示)。
(3)①下列可作为比较X和Y金属性强弱的依据是 (填序号)。
a.最高价氧化物的水化物的碱性 b.相应硫酸盐水溶液的pH
c.单质与水反应的难易程度 d.单质与酸反应时失去的电子数
②由X、Y、氢、氧四种元素所组成的化合物,能与盐酸以1:4反应生成两种常见盐和水,则该化合物的化学式为 。
(4)W的一种氢化物HW3可用于有机合成,其酸性与醋酸相似。体积和浓度均相等的HW3与X的最高价氧化物对应的水化物混合,混合后溶液中离子浓度由大到小的顺序是 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高二上期中测试化学试卷(解析版) 题型:选择题
下列关于Cl2性质的说法正确的是
A.密度比空气小 B.是无色无味的气体
C.能使干燥的有色布条褪色 D.可与NaOH溶液反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com