
关于甲、乙装置的下列叙述中正确的是

A.甲池中通甲烷的极是负极,溶液中Na+向Pt电极移动
B.C电极的电极反应为:O2+4e-+4H+==2H2O
C.乙池中的总反应为:Cu+H2SO4 H2
H2 +CuSO4
+CuSO4
D.反应过程中,甲、乙装置中溶液的pH都逐渐减小
C
【解析】
试题分析:A.甲池中通燃料甲烷的极是负极,根据同种电荷相互排斥,异种电荷相互吸引的原则,溶液中阳离子Na+向负电荷较多的正极C电极移动,错误;B.在燃料电池的正极C电极上发生还原反应,由于是碱性环境,所以正极上的电极反应为:O2+4e-+2H2O ==4OH-,错误;C.乙池中与电源的正极C连接的电极为阳极,发生反应:Cu-2e-=Cu2+,与电源的负极连接的Cu电极为阴极,发生反应:2H++2e-=H2↑,所以总反应为:Cu+H2SO4 H2↑+CuSO4,正确;D.反应过程中,甲装置的总方程式是:CH4+O2+2NaOH=Na2CO3+3H2O,不断消耗NaOH溶液,同时产生水,因此c(NaOH)碱性,溶液的pH逐渐减小,而对于乙装置,反应的总方程式是:Cu+H2SO4
H2↑+CuSO4,正确;D.反应过程中,甲装置的总方程式是:CH4+O2+2NaOH=Na2CO3+3H2O,不断消耗NaOH溶液,同时产生水,因此c(NaOH)碱性,溶液的pH逐渐减小,而对于乙装置,反应的总方程式是:Cu+H2SO4 H2↑+CuSO4,溶液的酸性逐渐减弱,所以溶液的pH逐渐增大,错误。
H2↑+CuSO4,溶液的酸性逐渐减弱,所以溶液的pH逐渐增大,错误。
考点:考查原电池、电解池的反应原理及应用的知识。
考点分析: 考点1:原电池 考点2:电解池 试题属性

 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案科目:高中化学 来源:2014-2015学年福建省福州市高三3月月考理综化学试卷(解析版) 题型:填空题
[化学一有机化学基础)(13分)芳香族化合物水杨酸、冬青油,、阿司匹林都是常用西药。它们的结构简式如下表:
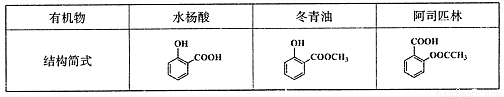
(1)水杨酸分子中式量较大的含氧官能团名称是 。
(2)水杨酸在浓硫酸催化作用下与乙酸酐(CH3C0)20反应生成阿司匹林,反应的化学方程 。
(3)水杨酸在一定条件下可以聚合成高分子化合物聚水杨酸,聚水杨酸的结构简式为: 。
(4)写出冬青油的一种同分异构体结构简式:异构体符合以下条件:
①芳香族化合物;
②苯环上一个氢原子被氯取代,有两种可能的产物;
③在足量氢氧化钠溶液中充分反应消耗等物质的量氢氧化钠。
(5)效更佳的长效缓释阿司匹林(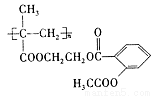 )在人体内可缓慢释放出阿司匹林分子,反应的化学方程式为 ,反应类型为 。
)在人体内可缓慢释放出阿司匹林分子,反应的化学方程式为 ,反应类型为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省商丘市高三第一次模拟考试化学试卷(解析版) 题型:选择题
在密闭容器中充入CO2、CO、CH4的混合气体共mg,若加入足量的Na2O2,充分振荡并不断用电火花引燃至反应完全,测得固体质量增加mg;则CO2、CO、CH4的体积比不可能为
A.1 :3 :1 B.1 :2 :1 C.1 :1 :1 D.1 :1 :2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市海淀区高三年级3月适应性训练理综化学试卷(解析版) 题型:选择题
已知反应:2NO2(红棕色) N2O4(无色)△H<0。将一定量的NO2充入注射器中后封口,下图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是
N2O4(无色)△H<0。将一定量的NO2充入注射器中后封口,下图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是

A.b点的操作是压缩注射器
B.c点与a点相比,c(NO2)增大,c(N2O4)减小
C.若不忽略体系温度变化,且没有能量损失,则T(b)>T(c)
D.d 点:v(正)>v(逆)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省枣庄市高三下学期开学初检测试卷理综化学试卷(解析版) 题型:推断题
选做(12分)【化学——有机化学基础】对羟基苯甲酸甲酯主要用作食品、化妆品、医药的杀菌防腐剂,以有机物M(分子式C9H10O2)为原料合成路线如下,其中E与 有图中所示转化关系(无机产物略):
有图中所示转化关系(无机产物略):

已知:当羟基与双键碳原子相连时,易发生转化RCH=CHOH RCH2CHO。
RCH2CHO。
请回答下列问题:
(1)B与F中具有相同的官能团,检验该官能团的试剂是 。上述变化中属于取代反应的是 (填反应编号)。
(2)写出结构简式M ,A 。
(3)写出下列反应的化学方程式:
反应⑤ ;D与碳酸氢钠溶液反应 。
(4)写出同时符合下列要求的M的同分异构体的结构简式 。
Ⅰ.含有苯环,且苯环上的一氯取代产物有3种
Ⅱ.能发生银镜反应和水解反应
Ⅲ.在稀氢氧化钠溶液中,1mol该同分异构体能与1molNaOH反应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省枣庄市高三下学期开学初检测试卷理综化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的数值,下列说法正确的是
A.10gNH3含有4NA个电子
B.0.1mol铁和0.1mol铜分别与0.1 mol氯气完全反应,转移的电子数均为0.2NA
C.标准状况下,22.4 L H2O中分子数为NA 个
D.1L 0.1 mol·L-1Na2CO3 溶液中含有 0.1NA个CO32-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省文登市高三第二次统考理科综合化学试卷(解析版) 题型:选择题
等质量的氯气与下列足量物质反应,转移的电子数最少的是
A.冷的NaOH溶液 B.SO2的水溶液
C.FeCl2溶液 D.铜
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省宁波市高三上学期期末考试化学试卷(解析版) 题型:填空题
(10 分)已知甲酸铜遇水易水解而具有还原性。实验室制备甲酸铜晶体[Cu(HCOO)2·4H2O]的流程如下:
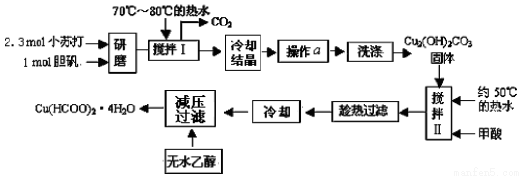
回答下列问题:
(1)研磨时应该将固体原料放在(填仪器名称) 中;制备 Cu2(OH)2CO3时需要用到70℃~80℃的热水溶解小苏打和胆矾的混合物,其目的是 。
(2)写出用小苏打、胆矾制备 Cu2(OH)2CO3的离子方程式 ;实际操作中的小苏打与胆矾 的物质的量之比大于 2∶1,原因是 。
(3)操作a 的名称是 。
(4)证明Cu2(OH)2CO3沉淀已经洗涤干净的实验方法是 。
(5)实验中用无水乙醇洗涤产物的目的是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省泰安市高三下学期一模理科综合化学试卷(解析版) 题型:填空题
对氮及其化合物的研究具有重要意义。
(1)在1 L密闭容器中,4 mol氨气在一定条件下分解生成氮气和氢气。2 min时反应吸收热量为46.1 kJ,此时氨气的转化率为25%。该反应的热化学方程式为_____________,这段时间内v(H2)=_________。
(2)298K时.在2L固定体积的密闭容器中,发生可逆反应:2NO2(g) N2O4(g)
N2O4(g)  =-akJ·mol-1(a>0),N2O4的物质的量浓度随时间变化如图所示。达平衡时,N2O4的浓度为NO2的2倍。
=-akJ·mol-1(a>0),N2O4的物质的量浓度随时间变化如图所示。达平衡时,N2O4的浓度为NO2的2倍。

①298K时,该反应的化学平衡常数为_________(精确到0.01);
②下列情况不是处于平衡状态的是__________(填字母序号);
a.混合气体的密度保持不变
b.混合气体的颜色不再变化
c.气压恒定时
③若反应在398K进行,某时刻测得n(NO2)=0.6 mol,n(N2O4)=1.2 mol,则此时v正____v逆(填“>”、“<”或“=”)。
(3)用氨气可设计成如图所示燃料电池,产生的X气体可直接排放到大气中。则a电极电极反应式为________________。
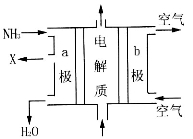
(4)t℃下,某研究人员测定NH3·H2O的电离常数为1.8×10-5。NH4+的水解常数为1.5×10-8,则该温度下水的离子积常数为___________,请判断t_____25℃(填“>”、“<”或“=”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com